плюсы и минусы метода, схемы лечения
 Современная медицина в курсе лечения герпеса принимает такую методику как супрессивное лечение – терапия, позволяющая забыть о самом заболевании и таких неприятных высыпаниях.
Современная медицина в курсе лечения герпеса принимает такую методику как супрессивное лечение – терапия, позволяющая забыть о самом заболевании и таких неприятных высыпаниях.
Какие препараты применяют в данном случае и на какие положительные результаты лечения можно рассчитывать – об этом и поговорим далее.
Содержание статьи
Подробнее о способе терапии
Большинство пациентов с вирусом герпеса в крови избавляются от его проявления на коже по мере высыпания последних, тем не менее, врачи говорят о более эффективном способе с такими неприятными признаками.
Супрессивное лечение герпеса – суть метода состоит в постоянном приеме определенных лекарственных препаратов, которые и подавляют сам вирус, не допуская развитие негативной симптоматики.
Данный метод терапии требует от пациента предельного внимания к принимаемым препаратам, самому курсу терапии — если прекратить их принимать после исчезновения негативной симптоматики, соответствующего положительного результата не будет. Помимо всего прочего – после прекращения приема препаратов симптомы герпеса проявляются еще сильнее. При должном соблюдении схемы приема препаратов – о герпесе можно позабыть.
Плюсы супрессивного лечения
Как отмечают врачи – принимать ретрогерпетические препараты можно принимать как в период обострения патологического процесса, так и достаточно долгий период времени. Среди преимуществ данной методы специалисты выделяют следующие пункты:
- В половине случаев можно говорить о полном выздоровлении и устранении вирусной инфекции герпеса или же частичных и непродолжительных обострениях, носящих скорее единичный, нежели системный характер.
- Если показывает себя рецидив или же обострение течения герпеса – протекают они легче и по времени непродолжительны, в меньшей степени беспокоит боль и неприятное жжение, зуд.
- Врачи отмечают, что даже в период ремиссии – пациент несет для своего окружения потенциальную угрозу заражения. В ходе применения методики супрессивного лечения такая вероятность снижается в разы и как следствие – риски заражения существенно уменьшаются.
- Поскольку вирус герпеса негативно влияет на иммунитет – при практике применения супрессивного лечения такое влияние снижается, иммунитет страдает меньше, восстанавливаясь.
Главными эффектами применения терапии супрессивного лечения специалисты называют:
- Улучшается качественная сторона жизни и осуществляется эффективный контроль над самим течением патологического процесса.
- Возможно в определенных случаях полное уничтожение в организме вирусной инфекции – такой положительный результат возможен только в том случае, если медикаментозная терапия применялась в первые сутки после заражения, пока вирус находиться в латентном своем состоянии.
- Снижается в разы высыпания вируса на кожных покровах, как и вероятность заражения пациентов окружающих его людей. Это избавляет не только от косметических проблем, но и психологического неудобства при диагностировании герпесного высыпания.
Минусы терапии
Поскольку данный метод терапии предусматривает длительный прием медикаментозных составов – лечение имеет и свои отрицательные стороны.
- В период прохождения курса лечения пациент может жаловаться на приступы рвоты и тошноты, боли в брюшине и вздутие живота.
- Редко, но может проявляться и диффузная аллопеция – частичное облысение у пациента и кожные по телу высыпания.
- Если препарат не подходит пациенту – показывают себя как побочный эффект сонливость и галлюцинация, заторможенность реакции.
- Боль и скованность мышц, судороги и аллергия, вплоть до наступления анафилактического шока и удушья.
В большинстве своем препараты, применяемые в курсе супрессивного лечения – не назначают беременным и в период лактации, поскольку компоненты могут через кровь или с молоком передаваться ребенку. Не назначают препараты и детям, не достигшим 3лет – в силу несформированной иммунной системы они могут нанести больше вреда, нежели пользы.
В период прохождения терапии – лучше всего не управлять машинами, не работать с механизмами, которые требуют повышенного от пациента внимания. Также важно принимать в расчет и тот факт, что при прохождении курса супрессивной терапии – вирус может показывать себя активными высыпаниями. Но это нормальная реакция на речение и частота обострения будет по мере лечения снижаться и полностью уходить.
Препараты для лечения
Перед началом прохождения курса супрессивной терапии стоит посетить врача – именно он и назначает лекарственные препараты, опираясь на результаты диагностических и лабораторных исследований. Узкопрофильными специалистами в данном вопросе есть дерматолог или же уролог, гинеколог – все зависит от места локализации высыпания, результатов диагностики и стадии течения патологического процесса.
По медицинской статистике – курс пройденной терапии позволяет на 80% снизить количество герпесных высыпаний и если ранее у пациента диагностировали за год 7-8 рецидивов, то по завершении пройденного курса лечения их число снижается до 1-2, а то и вовсе проходит.
Среди медикаментозных составов, применяемых в курсе супрессивной терапии, самыми эффективными специалисты называют — Ацикловир, Фамцикловир, Валацикловир или Валтреск, Бривудин и Фосканет. Представленные препараты имеют массу аналогов, отличающихся по стоимости, но незначительно разнящихся по составу и эффекту. Главное в курсе терапии – чем быстрее она будет назначена, тем лучше будут ее результаты. Помимо противовирусных препаратов курс терапии рекомендовано дополнить иммуномодуляторами и витаминами.

Чаще всего врачи назначают среди представленных препаратов Ацикловир или Валацикловир, Фамцикловир. Преимущества первого состоят в его доступной цене и незначительными побочными эффектами, хорошей переносимостью и возможностью назначать даже детям. Минус – для достижения положительной динамики лечения потребуется длительный курс приема препарата в силу низкой его биологической доступности.
В отношении Валацикловира, сильными сторонами препарата врачи называют высокую био-доступность и непродолжительность курса лечения для достижения положительной динамики лечения, всасываемость независимо от приема пищи и наименьшая его частота приема.
Сильными сторонами Фамцикловира врачи называют избирательное влияние на зараженные клетки и отсутствие негативного действия на здоровые, принимать его можно независимо от режима приема пищи, высокая биологическая доступность. Его минус — высокая стоимость.
Заключение
Подводя итог и резюмируя сказанное выше – применение методики супрессивного лечения показывает положительные результаты лечения и при правильно составленном курсе можно говорить о полном излечении.
Заместительная и супрессивная терапия в практике эндокринолога
Опубликовано в журнале:CONSILIUM MEDICUM »» ТОМ 11 / № 12
Е.А. Трошина, Н.В.Мазурина, Е.М.Скрынник
ФГУ Эндокринологический научный центр МЗСР РФ, Москва
Препараты тиреоидных гормонов относятся к числу наиболее часто используемых в клинической практике лекарственных средств. Их назначают с целью проведения заместительной или супрессивной терапии при ряде заболеваний щитовидной железы (ЩЖ).
Целью заместительной терапии является поддержание нормального обмена веществ у больных гипотиреозом любой этиологии.
Манифестный гипотиреоз
Левотироксин назначают из расчета 1,6–1,8 мкг на 1 кг массы тела (ориентировочная начальная доза для женщин 75–100 мкг/сут; мужчин – 100–150 мкг/сут).
Целевое значение тиреотропного гормона (ТТГ) при проведении заместительной терапии левотироксином первичного гипотиреоза составляет 0,5–1,5 мМЕ/л.
При проведении заместительной терапии центрального (вторичного) гипотиреоза необходимо добиться поддержания тироксина крови на уровне, соответствующем верхней трети нормальных значений для этого показателя.
Субклинический гипотиреоз
Тироксин назначают из расчета 1 мкг на 1 кг массы тела (ориентировочная начальная доза 50–75 мкг/сут).
Целью супрессивной терапии также является достижение концентрации ТТГ менее нижней границы нормы для предотвращения его возможного стимулирующего влияния на рост ткани ЩЖ (в том числе на рост резидуальной опухолевой ткани).
Целевое значение ТТГ составляет менее 0,1 мМЕ/л. Для этого используются дозы левотироксина от 2,2 до 2,5 мкг на 1 кг массы тела в сутки.
Принципы заместительной терапии левотироксином
Изменения секреции тиреоидных гормонов и снижение функции ЩЖ (гипотиреоз) могут происходить в результате поломки биосинтеза тиреоидных гормонов на разных его этапах: поступления йодида из крови, окисления его в элементарный йод, включения йода в состав тирозинов с образованием монойодтирозина и дийодтирозина, конденсации молекул йодтирозина с образованием Т4 и Т3. Независимо от того, на какой из стадий произошло нарушение метаболизма гормонов ЩЖ, будут изменяться те физиологические эффекты, за которые ответственны тиреоидные гормоны.
Основные физиологические эффекты тиреоидных гормонов:
• регуляция энергетического обмена
• регуляция роста и развития
• регуляция белкового, углеводного и жирового обмена
• влияние на сердечно-сосудистую систему
• влияние на костно-мышечную систему
• влияние на психику
Лечение всех форм гипотиреоза является заместительным и пожизненным. Исключение составляет только гипотиреоз, вызванный введением каких-либо медикаментов или веществ, блокирующих выработку тиреоидных гормонов.
Препараты левотироксина являются препаратами выбора для заместительной терапии гипотиреоза, и представляют собой синтетический тироксин (натриевая соль тироксина), который полностью идентичен тироксину, продуцируемому ЩЖ. Хорошо всасывается в желудочно-кишечного тракта (ЖКТ), причем при гипотиреозе его всасывание не нарушено.
Один из препаратов левотироксина – Эутирокс (фирма «Никомед»). Его отличием от других препаратов этой группы является возможность с легкостью подобрать нужную дозировку – 25, 50, 75, 100, 125 или 150 мкг, что существенно облегчает проведение как заместительной, так и супрессивной терапии.
На фоне заместительной терапии Эутироксом концентрация Т3 сохраняется постоянной. Режим дозирования препарата устанавливают индивидуально, с учетом тех возможных ситуаций, когда потребность в тироксине может изменяться (табл. 1).
Таблица 1. Ситуации, при которых может измениться потребность организма в тироксине
| Повышение потребности в тироксине | |
| • Снижение абсорбции в кишечнике (заболевания слизистой оболочки тонкой кишки и после операций на тонкой кишке) | |
| • Поносы при диабете | |
| • Цирроз печени | |
| • Беременность | |
| • Прием препаратов, снижающих абсорбцию | |
| Холестирамин Сукралфат Окись алюминия Сульфат железа | |
| • Препараты, увеличивающие выведение неметаболизированного Т4 | |
| Рифампицин Карбамазепин Возможно, фенитоин | |
| • Препараты, блокирующие конверсию Т4 в Т3 | |
| Амиодарон Дефицит селена | |
| Снижение потребности в тироксине | |
| • Пожилой возраст | |
| • Ожирение | |
Поскольку основной задачей лечения гипотиреоза является восстановление нормальных физиологических функций всех органов и систем, нарушенных вследствие гипотиреоза, то и при первичном, и при вторичном (третичном) гипотиреозе основа лечения – адекватная заместительная терапия препаратами тиреоидных гормонов. Критерием адекватности лечения служит исчезновение клинических и лабораторных проявлений гипотиреоза.
Компенсация манифестного гипотиреоза – 1,6–1,8 мкг левотироксина в сутки. Средняя суточная доза 75–150 мкг
Компенсация субклинического гипотиреоза – 1 мкг левотироксина на 1 кг массы тела. Средняя суточная доза 50–75 мкг
Терапию начинают с небольшой дозы Эутирокса, причем у пожилых она может составлять 12,5 мкг/сут. Препарат принимают утром, натощак. Дозу постепенно увеличивают до поддерживающей (у молодых больных за 4 нед, у пожилых за 2 мес, а иногда, при наличии сопутствующей кардиальной патологии, за 3–4 мес).
Оценивать уровень ТТГ на фоне лечения следует не раньше чем через 2 мес от начала терапии. Далее исследовать этот показатель нужно с интервалом 1 раз в 6 мес и корректировать дозу Эутирокса в зависимости от полученных результатов.
При лечении вторичного гипотиреоза схема назначения препарата аналогичная, однако контролировать, по понятным причинам, следует не ТТГ, а свободный Т4. В табл.2 представлен начальный этап лечения гипотиреоза.
Таблица 2. Начальный этап заместительной терапии у больных гипотиреозом
| Больные без кардиальной патологии моложе 65 лет | |
| Левотироксин назначают из расчета 1,6–1,8 мкг на 1 кг массы тела | |
| Ориентировочная начальная доза: | |
| • женщины – 50–75 мкг/сут | |
| • мужчины – 75–100 мкг/сут | |
Больные с кардиальной патологией и/или старше 65 лет
Начальная доза 12,5 мкг левотироксина в день (увеличивать по 12,5 мкг с интервалом 2 мес до нормализации уровня ТТГ, при появлении или ухудшении кардиальных симптомов провести коррекцию терапии).
Тяжесть и длительность гипотиреоза являются основными критериями, определяющими тактику врача в момент начала лечения.
Чем тяжелее гипотиреоз и чем дольше он был некомпенсирован, тем выше будет общая восприимчивость организма к тиреоидным гормонам, особенно это относится к кардиомиоцитам. Поэтому процесс адаптации к препарату должен быть постепенным и плавным независимо от возраста пациента.
При назначении тироксина пациенту с гипотиреозом нужно выяснить, какие еще медикаменты он получает, поскольку многие препараты могут увеличивать потребность в тироксине. Если не учитывать этот эффект, компенсация гипотиреоза может быть затруднена.
Субклинический гипотиреоз характеризуется отсутствием четких клинических проявлений заболевания. Жалобы пациента, как правило, неспецифичны и часто сводятся к повышенной слабости и утомляемости. Лабораторные параметры включают в себя незначительное повышение ТТГ при нормальных уровнях Т3 и Т4. Нередко субклинический гипотиреоз является случайной находкой при общем обследовании больного. Данный синдром чаще обнаруживается у пожилых пациентов.
Для верификации диагноза нужно провести больному повторное определение уровня ТТГ через 6 мес. В том случае, если у пациента регистрируется стойкое повышение уровня ТТГ, вопрос о лечении следует решать в индивидуальном порядке. Однозначного мнения по поводу целесообразности специфической терапии субклинического гипотиреоза в настоящее время нет. Но если такая терапия проводится, то она должна сопровождаться адекватным и своевременным наблюдением за пациентом, включающим в себя определение уровня ТТГ. Как правило, заместительную терапию при субклиническом гипотиреозе начинают тогда, когда уровень ТТГ составляет 10 мЕ/л и выше, и Эутирокс назначают в дозе 1 мкг на 1 кг массы тела (суточная доза составляет 50–75 мкг).
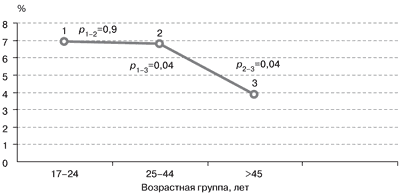
| Рис. 1. Распространенность ДЗ в различных возрастных группах. |
 |
Гипотиреоз и беременность
При некомпенсированном гипотиреозе наступление беременности крайне маловероятно. Если беременность все же наступила, то лечение гипотиреоза должно быть начато немедленно. Во время беременности потребность в левотироксине в среднем возрастает на 45% от расчетной исходной дозы. Если беременность наступила у женщины с компенсированным гипотиреозом, то доза препарата должна быть увеличена в соответствии с возросшей потребностью в нем.
Принципы супрессивной терапии левотироксином
Высокодифференцированный рак ЩЖ (ВДРЩЖ)
На протяжении многих лет основным способом терапии для больных, получивших радикальное лечение по поводу ВДРЩЖ, остается введение тиреоидных гормонов в дозах, превышающих физиологические (2,5 мкг на 1 кг массы тела в сутки), с целью снижения концентрации сывороточного ТТГ. Клетки рака ЩЖ, происходящие из фолликулярного эпителия, имеют рецепторы ТТГ, и в ответ на их стимуляцию происходит повышение активности аденилатциклазы. Предполагается, что эти опухоли ЩЖ могут расти под воздействием ТТГ. Многие исследователи отмечали уменьшение частоты рецидивов опухолевого роста благодаря подавлению секреции ТТГ под воздействием супрессивной терапии как при папиллярной, так и при фолликулярной тиреоидной карциноме.
Сегодня рекомендуется использовать методы анализа ТТГ III поколения, которые позволяют выявлять его присутствие в сыворотке в концентрациях порядка 0,01 мЕд/л.
До сих пор активно обсуждается вопрос о том, что более опасно для пациента: предотвращение рецидива рака при условии поддержания субклинического тиреотоксикоза или неблагоприятное влияние медикаментозного тиреотоксикоза на сердце и кости. Побочные эффекты супрессивных доз левотироксина включают нарушения контрактильности миокарда, увеличение частоты сердечных сокращений и предсердные аритмии, а также могут вызывать ускорение круговорота элементов костной ткани, остеопороз. По этой причине многие специалисты считают, что полное подавление секреции гипофизарного ТТГ на протяжении длительного периода (до 0,01–0,1 мЕд/л или ниже) целесообразно лишь у больных, входящих в группу высокого риска – в первую очередь при повышенной вероятности рецидивов или смерти у пациентов с ВДРЩЖ. В то же время большинство клиницистов полагают, что у подавляющего числа больных с папиллярной тиреоидной карциномой, относимых к группе низкого риска на основании результатов прогностической балльной оценки, хороший эффект дает относительно слабое подавление секреции ТТГ. У таких больных концентрацию сывороточного ТТГ следует поддерживать на уровне 0,1–0,4 мЕд/л. В целом при лечении ВДРЩЖ, по имеющимся на сегодняшний день данным контролируемых исследований, назначение высоких доз левотироксина с целью подавления уровня ТТГ имеет преимущества по сравнению с обычной заместительной терапией, при которой поддерживается эутиреоз, т.е. нормальный уровень ТТГ. Исключение могут составлять пожилые больные или больные с тяжелым заболеванием сердца и выраженным остеопорозом.
- У пациентов низкого риска без признаков заболевания через год терапии доза Эутирокса может быть снижена для поддержания уровня ТТГ в сыворотке крови на уровне нижней границы диапазона нормальных значений (0,5–1,0 мЕд/л).
Узловой коллоидный зоб
В настоящее время в соответствии с Консенсусом РАЭ решение вопроса о целесообразности супрессивной терапии левотироксином при узловом коллоидном зобе определяется в индивидуальном порядке. Лечение препаратами тироксина наиболее эффективно при солитарных коллоидных узлах паренхиматозного типа строения, сочетающихся с увеличением ЩЖ и/или наличием в ткани железы зобных изменений, определяемых при ультразвуковом исследовании(УЗИ).
Левотироксин в лечении диффузного нетоксического зоба
Диффузный нетоксический зоб
Диффузный нетоксический зоб – общее диффузное увеличение щитовидной железы без нарушения ее функции. Основной причиной диффузного зоба является недостаточное содержание йода в окружающей среде и как следствие сниженное его потребление населением с привычными продуктами питания. В зависимости от распространенности диффузного зоба (ДЗ) в популяции различают спорадический и эндемический зоб. Зоб считается эндемическим, если в обследуемом регионе частота встречаемости зоба у детей младшего и среднего школьного возраста составляет более 5%. Хотя в подавляющем большинстве случаев причиной ДЗ является недостаточное поступление в организм человека йода, ряд закономерностей позволяет предположить о влияние генетических факторов на его формирование. Обращает на себя внимание тот факт, что в одном и том же регионе при одном и том же йодном обеспечении зоб определяется не у всего населения, а лишь у части. Важность генетических факторов подтверждена многими популяционными, семейными и близнецовыми исследованиями. Кроме того, при ДЗ выявлены некоторые мутации в таких генах, как ТРО, NIS, TG, TSHR.
Известно, что распространенность любых форм зоба в популяции существенно различается в зависимости от возраста. Считается, что ДЗ как первая стадия йододефицитного заболевания чаще встречается у молодых людей. Этот факт нашел свое подтверждение и на территории Москвы – зоны легкого йодного дефицита, при сравнении частоты встречаемости ДЗ в различных возрастных группах взрослого населения (рис. 1).
ДЗ достоверно чаще встречался у лиц моложе 45 лет.
Хотя пациенты с ДЗ, как правило, не предъявляют жалоб, функция ЩЖ у них не нарушена, они все же нуждаются в лечении данного заболевания, поскольку оно является первой фазой(обратимой при правильном лечении) формирования узлового и многоузлового йододефицитного зоба, в том числе и с развитием синдрома тиреотоксикоза на поздних стадиях процесса.
На сегодняшний день существует три варианта консервативной терапии ДЗ:
- Монотерапия левотироксином (Эутирокс).
- Монотерапия препаратами йода (Йодбаланс).
- Комбинированная терапия препаратами йода и левотироксина.
Как было сказано, назначение левотироксина широко применялось для лечения эутиреоидного ДЗ в прошлом. При этом на начальном этапе достигались отличные результаты. Во многих клинических исследованиях было показано, что уже через 3–4 мес от начала терапии происходило значительное (не менее 20%) уменьшение объема железы. Чаще же всего в клинической практике использовались дозы 150 мкг у взрослых и 100 мкг у подростков. Однако в многочисленных работах однозначно продемонстрирован «феномен отмены» – увеличение размеров ЩЖ почти до исходного уровня через короткое время после прекращения лечения. Данный феномен объясняется прежде всего тем, что при подавлении ТТГ снижается активность Na-I симпортера, а следовательно, уменьшается активный захват йода ЩЖ. На фоне резкого падения интратиреоидного содержания йода при отмене лекарственного препарата происходит новый рост железы. Также к нежелательным побочным явлениям терапии гормонами ЩЖ относят возможное возникновение лекарственного тиреотоксикоза, тахиаритмии, остеопороза, что ограничивает использование этой группы препаратов при длительном лечении ДЗ. Однако иногда для быстрого достижения терапевтического эффекта прибегают к кратковременному курсу лечения ДЗ Эутироксом с дальнейшим переходом на поддерживающую терапию Йодбалансом.
Рис. 2. Динамика объема ЩЖ в группе «Монотерапия препаратом йода» исходно, на 8 и 12-м месяце. 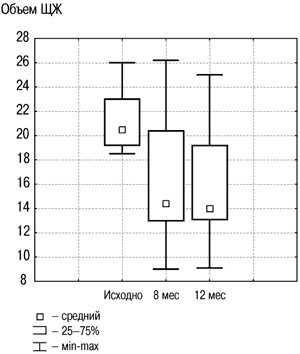
Рис. 3. Динамика объема ЩЖ в группе «Комбинированная терапия» исходно, на 8 и 12 месяце. 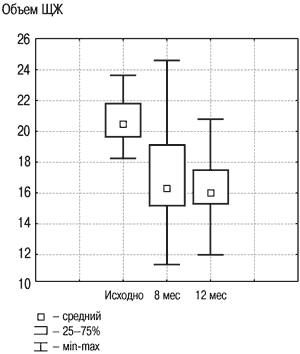
Таблица 3. Сравнение основных показателей между группами «Монотерапия» и «Комбинированная терапия» через 12 мес
| Показатель | Монотерапия | Комбинированная терапия | р (критерий) |
| Объем ЩЖ | 16,1 (13,1; 19,2) | 16,1 (15,2; 17,5) | 0,83 (Рм-у=0,21) |
| ТТГ | 0,9 (0,8; 1,1) | 1,2 (1; 1,48) | 0,07 (Рм-у=0,92) |
| АТ к ТПО*, % | 3 | 0 | 1 |
Монотерапия препаратом йода и комбинированная терапия
Наиболее предпочтителен метод лечения ДЗ, являющийся этиологическим. Препараты йода назначают в физиологических дозировках (200 мкг в сутки) на 6 мес с последующей оценкой динамики объема ЩЖ.
При отсутствии выраженного эффекта от приема йодидов через 6 мес может быть рекомендован переход на комбинированную терапию. При этом предпочтение должно отдаваться либо фиксированной комбинации 75 мкг левотироксина +150 мкг йодида, либо индивидуально подобранной дозе Эутирокса из расчета 1 мкг на 1 кг массы тела в сочетании с 150 мкг йодида в сутки.
В настоящее время клиницисты имеют возможность использовать в этих целях комбинированные препараты, в состав которых входит как левотироксин, так и йод. Так, препарат Йодтирокс («Никомед») оптимально сочетает левотироксина натрий – 100 мкг и калия йодид – 100 мкг. Суточную дозу Йодтирокса принимают 1 раз в день утром, натощак, за 30 мин до завтрака, запивая таблетку небольшим количеством жидкости и не разжевывая.
Комбинированная терапия препаратами йода и тироксина, как было неоднократно показано, имеет ряд преимуществ. Во-первых, воздействуя на несколько патогенетических механизмов образования зоба, подавляется и гипертрофия, и гиперплазия тиреоцитов. Это позволяет добиться результатов, по эффективности сопоставимых с монотерапией тироксином (при гораздо меньшем его содержании), что в свою очередь уменьшает количество побочных эффектов, связанных с приемом тиреоидных препаратов. Во-вторых, снижается также склонность к «эффекту отмены» при кратковременном перерыве в лечении. В-третьих, менее выражено подавление уровня ТТГ, например по сравнению с эффектом тироксина в дозе 150 мкг.
Результаты исследования динамики объема ЩЖ у лиц с ДЗ на фоне разных схем терапии, проведенного в ФГУ ЭНЦ, представлены на рис. 2, 3. В целом по группе объем ЩЖ уменьшился на 20% к моменту завершения лечения, что явилось статистически значимым (р1–2<0,001), и продолжал удерживаться примерно на том же уровне спустя еще как минимум 4 мес после его прекращения (р2–3=0,31). Случаев изменения функции ЩЖ (развития гипер- и гипотиреоза) отмечено не было, колебания уровня ТТГ не выходили за пределы нормальных значений.
В данной группе объем ЩЖ в среднем снизился на 20,6% через 8 мес лечения, что было значимо относительно начала лечения (р1–2<0,001), и оставался на том же уровне через 4 мес спустя после его отмены (р2–3<0,77). Субклинический тиреотоксикоз был выявлен у 1 пациента на 8-м месяце наблюдения (ТТГ–0,01 мЕд/л, свободный Т4–19 пмоль/л). В целом по группе уровень ТТГ не выходил за пределы нормальных значений на протяжении всего периода наблюдения.
При использовании анализа повторных изменений было показано, что как в группе «Монотерапия», так и в группе «Комбинированная терапия» объем ЩЖ уменьшился до нормы на фоне 8-месячного лечения и оставался примерно на том же уровне спустя 4 мес после лечения. Для оценки преимущества одного метода лечения перед другим изучаемые параметры обеих групп были сравнены между собой (см. табл. 2).
При сравнении показателей между группами на 8 и 12-м месяцах наблюдения статистически значимой разницы между уменьшением объема ЩЖ, уровнем ТТГ, АТ к ТПО не обнаружено. Таким образом, и монотерапия препаратами калия йодида, и комбинированная терапия препаратами калия йодида и левотироксина в равной степени эффективны и безопасны для лечения эутиреоидного ДЗ. Также было показано, что результат лечения ДЗ с использованием монотерапии препаратами йода может зависеть от генетических факторов: носители генотипов АА и АС полиморфного маркера rs 3783949 гена TSHR чаще имели удовлетворительный результат лечения, носители генотипа СС – неудовлетворительный результат. Результат лечения ДЗ при помощи комбинированной терапии не зависел от распределения полиморфных маркеров генов TSHR (rs 3783949, замена – A/С), NIS (rs 7250346, замена – C/G), DUOX1(rs2467825, замена – A/G) DUOX2 (rs7171366, замена – G/T), TPO (rs 17091737, замена – G/T).
Заключение
Решение о начале заместительной или супрессивной терапии препаратами левотироксина (Эутирокс) или комбинированной терапии (Йодтирокс) должно быть обосновано данными клинического и лабораторного обследования пациента. Несмотря на наличие вполне определенных алгоритмов назначения препарата и режима его дозирования, всегда следует учитывать индивидуальные особенности пациента в каждом конкретном случае во избежание возможных побочных эффектов от назначаемого лечения.
Литература
- Charib H, Mazzferri EL. Thyroxine suppressive therapy in patients with nodular thyroid disease. Am Internat Metabol 1998; 128: 386–94.
- Cooper DS, Specker B, Ho M et al. Thyrotropin suppression and disease progression in patients with differentiated thyroid cancer: results from the National Thyroid Cancer Treatment Cooperative Registry. Thyroid 1998; 8: 737–44.
- Cobin RH. Thyroid hormone excess and bone a clinical review. Endocrin Practical 1995; 1: 404–9 .
- Hay ID, McConahey WM, Goellner JR. Managing patients with papillary thyroid carcinoma: insights gained from the Mayo Clinic’s through 2000. Trans American Clinical Clim Assoc 2000; 113: 241–60.
- Hundahl SA, Cady B, Cunningham MP et al. Initial results from a prospective cohort study of 5583 cases of thyroid carcinoma treated in the United States during 1996. J Cancer 2000; 89: 202–17.
- Kaplan MM. (Ed). Thyroid carcinoma. Endocrinology and Mrtatabolis. Clin North Am 1990; 19: 469–766
- Mazzaferri EL, Jhiang SM. Long term impact of intial surgical and medical therapy on papillary and follicular thyroid cancer. Am J Med 1994; 49: 418–28.
- Mazzaferri EL, Jhiang SM. Long-term impact of initial surgical and medical therapy on papillary and follicular thyroid cancer. Am J Med 1994; 97: 418–28.
- Esnajla NF, Cantor SB, Sherman SI et al. Optimal treatment strategy in patientswith papillary thyroid cancer: A decision analysis. J Surg 2001; 130: 921–30.
- Wilders-Truschnig MM, Warnkross H, Leb G. The effect of treatment with levothyroxine or iodine on thyroid size and thyroid growth stimulating immunoglobulins in endemic goiter patients. Clin Endocrinol (Oxf.) 1993; 39 (3): 281–6 .
- Kreissl M, Tiemann M, Hanscheid H. Comparison of the effectiveness of two different dosages of levothyroxine-iodide combinations for the therapy of euthyroid diffuse goiter. Dtsch Med Wochenschr 2001; 126 (9): 227–31.
- Галкина Н.В., Мазурина Н.В., Трошина Е.А. Гены-кандидаты тиреоидной патологии. Клин. и эксперим. тиреодол. 2006; 1: 10–4 .
- Трошина Е.А., Н.В.Галкина, Мазурина Н.В., Мартиросян И.Т. Структурные изменения щитовидной железы: результаты скринингового ультразвукового обследования населения Москвы. Пробл. эндокринол. 2005; 51 (5): 36–9 .
- Трошина Е.А., Мазурина Н.В., Галкина Н.В. Диффузный эутиреоидный зоб: эпидемиология, диагностика, лечение: болезни щитовидной железы. Cons Med 2005; 7 (9): 769–73.
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Супрессивная терапия при раке щитовидной железы
Что такое супрессивная терапия?
Супрессивная терапия — это медикаментозное лечение, направленное на подавление каких-либо процессов в организме. Супрессивная терапия при раке щитовидной железы подразумевает собой корректировку концентрации тиреотропного гормона, вырабатываемого гипофизом.
ТТГ – важный гормон, участвующий в функционировании щитовидной железы. Он стимулирует синтез трийодтиронина и тироксина, необходимых для правильной работы внутренних органов, метаболических процессов и поддержания психических функций человека.
Также ТТГ участвует в синтезе белков, фосфолипидов, нуклеиновых кислот, тем самым стимулирует рост и количество тиреоидных клеток. Если уровень тиреотропного гормона выше, чем необходимо, то развивается гипертрофия тканей щитовидной железы и содержание в ней коллоида.
Доказано, что тиреотропный гормон стимулирует рост и деление клеток дифференцированных раковых опухолей. Поэтому при папиллярном и фолликулярном раке щитовидной железы необходимо снижение концентрации ТТГ.
Супрессивная терапия при раке щитовидной железы проводится с помощью препаратов левотироксина – синтетического аналога тироксина. Большие дозировки этого препарата подавляюще действуют на гипофиз, который начинает продуцировать меньшее количество ТТГ.
Внимание! Уровень Т4 и ТТГ находится в обратно пропорциональной зависимости – чем выше уровень Т4, чем ниже становится ТТГ, и если концентрация Т4 падает, то уровень тиреотропного гормона начинает стремительно расти.
Показания к проведению супрессивной терапии
Супрессивная терапия при раке щитовидной железы показана пациентам с папиллярными и фолликулярными опухолями. При анапластическом и медуллярном раке данный метод лечения неэффективен, поэтому препараты левотироксина могут назначаться только после тиреоидэктомии в качестве заместительного лечения.
Назначение супрессивной терапии необходимо пациентам с дифференцированными видами рака, после удаления опухоли. Большие дозы левотироксина препятствуют повторному образованию злокачественных опухолей в тиреоидной ткани и проникновению раковых частиц в лимфатические протоки и системный кровоток.
Показания:
- профилактика рецидива после удаления дифференцированной опухоли;
- обнаружение раковых узлов менее 4 см., после гемитиреоидэктомии, проводимой по удалению доброкачественных образований;
- обнаружение «горячих» очагов на сцинтиграфии после удаления раковых опухолей;
- профилактика развития рака при наличии фолликулярных аденом;
- любые гиперпластические изменения щитовидной железы, имеющие высокую склонность к перерождению в злокачественные опухоли.
Если после операции по удалению доброкачественных и злокачественных опухолей щитовидки, наблюдается высокой уровень тиреотропного гормона, считается, что болезнь имеет высокую склонность к перерождению в злокачественный процесс. В таком случае лечение большими дозами левотироксина требуется в качестве профилактики.
Принципы проведения супрессивной терапии
Супрессивная терапия проводится так же, как и заместительная – пациенту прописывают синтетические аналоги Т4 для ежедневного приема. Но при подавляющем лечении подбирается более высокая дозировка препарата, которая зависит от концентрации ТТГ в сыворотке крови.
Внимание! Особенно важно подавлять продуцирование ТТГ больным с агрессивными и активно метастазирующими опухолями.
Существует несколько принципов, которым должна соответствовать супрессивная терапия:
- Не может использоваться, как единственный метод лечения рака щитовидной железы. Вспомогательные мероприятия подбираются в зависимости от тяжести заболевания и общего состояния пациента. При наличии метастазов и высоком риске рецидива чаще используют лечение радиоактивным йодом.
- Эффективность лечения можно отследить не ранее, чем через три месяца после начала приема гормонального средства.
- Сдавать анализы для определения концентрации тиреотропного гормона следует один раз в 3 месяца в течение первого года, затем при наличии положительного результата, анализы сдаются 1-2 раза в год.
- Во время лечения регулярно исследуется щитовидная железа с помощью УЗИ и проводится радиоизотопное исследование организма.
- Принимать препараты левотироксина нежелательно одновременно с другими лекарствами – нужно выждать не менее 2 часов, чтобы не нарушить всасываемость гормона в системный кровоток.
- При необходимости приема других лекарственных средств, необходимо проконсультироваться с врачом, возможно, что потребуется корректировка дозировки.
- Необходимо учитывать, что левотироксин снижает действие инсулина и некоторых сердечных препаратов, а также усиливает влияние антикоагулянтов и трициклических антидепрессантов.
- Следует принимать синтетический аналог Т4 одной и той же марки, так как при смене производителя возможно снижение или повышение уровня ТТГ в течение 50 дней после замены препарата.
Чаще всего подавление тиреотропного гормона препаратами левотироксина проводится пожизненно.
Лишь в некоторых случаях врач может скорректировать дозировку и перевести больного на гормонозаместительное лечение:
- Если радиоизотопная диагностика после тиреоидэктомии фолликулярной или папиллярной опухоли на протяжении 15 лет показывает отсутствие прогрессирования болезни.
- При фолликулярных и папиллярных карциномах размером менее 2 см., если на протяжении 10 лет не было рецидива и метастазирования.
- Если пациенты находятся в группе низкого или очень низкого риска повторного развития болезни.
Пожизненная супрессивная терапия требуется людям старше 65 лет, а также больным, кому была удалена опухоль четвертой стадии. Довольно часто пожизненный прием левотироксина в больших дозировках требуется детям и подросткам после удаления злокачественных опухолей щитовидной железы.
Норма уровня гормонов при терапии
Чтобы подобрать дозировку синтетических гормонов для подавления продуцирования тиреотропного гормона, необходимо пройти обследование и сдать кровь на анализы. Чем выше концентрация ТТГ, чем больше первоначальная дозировка левотироксина. В процессе лечения дозировка постоянно корректируется — это зависит от результатов анализов, которые пациент должен сдавать регулярно.
В норме у здорового человека концентрация тиреотропного гормона составляет 0,5-5 mU\l. Но это слишком большое количество ТТГ, способное стимулировать опухолевидные клетки тиреоидной ткани. Поэтому цель супрессивной терапии добиться значительного снижения тиреотропного гормона.
Пациентам, находящимся в группе низкой вероятности рецидива, рекомендуется поддерживать концентрацию ТТГ в пределах 0,1-0,5 mU/l. При агрессивных опухолях и высокой вероятности развития рецидива, уровень тиреотропного гормона не должен быть выше 0,1 mU/l. Больным, имеющим длительный период ремиссии и считающимся клиническими излеченными, допустимо поддерживать уровень ТТГ в пределах 0,3-2,0 mU/l.
Внимание! Низкий риск рецидива ставится при стадиях T1N0M0 или T2N0M0. О высоком риске говорят при стадиях T3 или T4, а также любом Т в сочетании с N1 или M1, то есть при наличии региональных и отдаленных метастазах.
Супрессивная терапия при раке щитовидной железы требует постоянного контроля над уровнем ТТГ. Если уровень тиреотропного гормона станет выше необходимой нормы, то повышается риск образования вторичной опухоли и распространения метастазов по отдаленным участкам тела. В таком случае прогноз выживаемости пациента значительно снижается. Именно поэтому важно подобрать правильную дозировку препарата и регулярно ее корректировать.
Кому не назначают супрессивную терапию?
Супрессивная терапия после операции на щитовидной железы по удалению злокачественной опухоли не проводится, если гистология показала наличие медуллярных или анапластических клеток. Эти виды рака не лечатся с помощью гормонов, но хорошо поддаются химиотерапии и облучению радиоволнами.
Также учитываются общее состояние пациента, особенно функционирование сердечно-сосудистой системы. Если наблюдаются выраженные нарушения сердечного ритма, стенокардия или хроническая гипертония, то прием высоких доз левотироксина может значительно ухудшить состояние пациента.
Если наблюдаются абсолютные противопоказания к супрессивной терапии, то лечащий врач, по возможности, старается оставить небольшой участок тиреоидной ткани, чтобы организм больного смог вырабатывать необходимое для жизни количество гормонов щитовидки.
Побочные эффекты супрессивной терапии
Супрессивная терапия после удаления щитовидной железы при правильно подобранных дозировках редко вызывает побочные эффекты и хорошо переносится большинством пациентов. Но при индивидуальной непереносимости возможно появление аллергических реакций, кожной сыпи, зуда.
Чрезмерное количество принимаемого препарата приводит к тиреотоксикозу, сопровождающемуся судорогами, головными болями, повышенной раздражительностью, болями в груди, дисменореей и расстройством стула. В очень редких случаях после тиреоидэктомии, если была назначена слишком низкая дозировка левотироксина, появляются симптомы гипотиреоза: слабость, апатия, постоянная сонливость, резкое увеличение массы тела, запоры, мышечные боли. У детей на фоне левотироксина появляются мучительные головные боли – псевдоопухоль мозга.
Супрессивная терапии при раке щитовидной железы требует приема больших дозировок синтетических аналогов тироксина, что через несколько лет приема может вызвать достаточно серьезные последствия.
Препарат нарушает работу сердечно-сосудистой системы, что выражается следующими симптомами:
- боли в области сердца;
- тахикардия;
- аритмия;
- экстрасистолия;
- гипертрофия отделов сердца;
- высокое артериальное давление.
Если появляются выраженные отклонения в работе сердечно-сосудистой системы, то пациента направляют на полное кардиологическое обследование, после чего решается вопрос о снижении дозировки Левотироксина.
Второе по частоте осложнение – остеопороз, которому наиболее предрасположены дети, подростки, а также женщины в период постменопаузы. Заподозрить наличие остеопороза можно по следующим симптомам: ломкость ногтей, боли в суставах, искривление позвоночника и частные переломы костей. Чтобы определить остеопороз на ранней стадии необходимо регулярно сдавать анализы на кальций, фосфор, остеокальцин и паратгормон.
Будьте здоровы!
Супрессивная терапия для профилактики рецидивов рака щитовидки
Стандартный курс лечения хорошо дифференцированных типов рака щитовидки, как правило, состоит из лазерной абляции, химической или лучевой терапии, хирургической операции.
Супрессивная терапия, или метод искусственного подавления тиреотропного гормона, используется в сочетании с другими видами терапии для того, чтобы предотвратить возобновление роста раковых клеток в щитовидной железе.
Супрессивная терапия доказала свою эффективность в лечении рецидивов рака и злокачественных опухолей с высокой степенью риска метастазирования. В статье подробно рассказано о том, что такое супрессивная терапия, кому она противопоказана и как контролировать показатели гормонов.
Зная, в каких случаях назначается терапия подавления тиреотропного гормона щитовидки и как она работает, можно не только подготовиться к неприятным последствиям, но и настроиться на полное выздоровление.
Что такое супрессивная терапия?
Супрессивная (превентивная или подавляющая) терапия — это часть комплексной программы борьбы с раком щитовидки.
Этот метод лечения используется для
предотвращения роста новых злокачественных опухолей после удаления основного очага рака.
Терапия также используется для предотвращения распространения микроскопических опухолей, которые не могут быть обнаружены и удалены.
Стоит знать, что превентивная терапия идеально подходит для профилактики рецидивов хорошо дифференцированных видов рака. Но для лечения анапластического типа рака супрессивная терапия не назначается, так как её эффективность все еще не доказана.
Принципы супрессивной терапии
Пациентам, перенесшим курс лечения дифференцированных типов рака щитовидки (папиллярного, фолликулярного), необходимо ежедневно принимать синтетические гормоны.
Таблетки под названием левотироксин (также известный как Т4) назначают для того, предотвратить гипотиреоз (пониженная выработка гормонов щитовидки) и рецидив раковой болезни.
Как правило, пациент получает достаточно большую дозу Т4 для того, чтобы значительно снизить уровень тиреотропного гормона в крови.
Подавление выработки ТТГ очень важно в тех случаях, когда у больного диагностирована активно метастазирующая или очень агрессивная опухоль.
В таких случаях супрессивная терапия назначается после хирургической операции в комплексе с приемом радиоактивного йода.
Около 85% пациентов полностью излечиваются от раковой болезни после хирургического удаления опухоли.
Успешные результаты лечения подтверждаются путем определения уровня тиреоглобулина в крови.
Как только диагност подтверждает, что пациент полностью освободился от раковой опухоли, проводится гормонограмма, по результатам которой определяется необходимость супрессивной терапии.
Пациенты, которые перенесли полное хирургическое удаление щитовидки, должны принимать препараты левотироксина всю жизнь. В данном случае, супрессивная терапия необходима для поддержания полноценной здоровой жизни человека.
Препараты левотироксина выпускаются в форме таблеток. Принимать их необходимо на пустой желудок (желательно с утра).
Как правило, левотироксин не рекомендуют принимать с другими препаратами, так как большое количество медикаментов препятствует быстрому попаданию синтетических гормонов щитовидки в кровоток.
С осторожностью следует комбинировать
левотироксин с витаминами, цинком железом.
Необходимо согласовать с фармацевтом и эндокринологом график приема гормонов и комбинацию Т4 с любыми другими необходимыми препаратами.
Существует несколько марок-синонимов левотироксина. Обычно эндокринологи рекомендуют пациентам принимать препараты одной и той же индивидуально подобранной марки.
Доказано, что если сделать анализ крови через 50 дней после смены марки препарата, уровень ТТГ может значительно измениться.
Норма уровня гормонов при терапии
Необходимое количество Т4 определяется индивидуально для каждого отдельного пациента, но существует несколько общих рекомендаций относительно контроля уровня гормонов.
При первоначальном проведении супрессивной терапии, сразу после окончания основного курса лечения щитовидки, онкологи рекомендуют не повышать количество ТТГ в крови до 0,1 мЕд/л.
Если же риск рецидива рака сводится к минимуму, то следует скорректировать уровень гормона до границ нормы (0,1-0,5 мЕд/л ).
При назначении долгосрочной супрессивной терапии, эндокринологи советуют придерживаться следующих рекомендаций:
- Больным с высоким риском метастазирования опухоли или рецидива заболевания, ТТГ нужно поддерживать на уровне близкому к 0.1 мЕд/л., при условии отсутствия конкретных противопоказаний.
- Пациентам, которые прошли курс химио или радиотерапии, при невысоком риске наличия остаточных метастаз, следует уделять внимание поддержанию ТТГ на уровне 0.1-0.5 мЕд/л.
- По прошествии 9-10 лет, при условии полного отсутствия метастаз, количество принимаемого левотироксина можно незначительно снизить.
- У пациентов с очень низким риском рецидива, уровень тиреотропного гормона необходимо поддерживать в пределах нормального диапазона у здорового человека (0.5-0,8 мЕд/л).
- Пациентам, у которых в течение 10 лет не было обнаружено никаких остаточных злокачественных клеток, количество принимаемого левотироксина можно свести к минимуму. Допустимый уровень ТТГ может подняться на верхней границе нормы (0.8-1,2 мЕд/л).
Кому не назначают супрессивную терапию?
Как отмечалось ранее, злокачественная недифференцированная карцинома не подвергается стандартному лечению. Таким образом, и супрессивная терапия, направленная на подавление тиреотропного гормона, не является эффективной.
Клинических доказательств эффективности супрессивной терапии также недостаточно для проведения успешной профилактики рецидивов медуллярного рака.
Если риск появления метастазов достаточно низкий, то онколог может принять решение о частичной резекции пораженной доли щитовидки.
Таким образом, хирург оставит одну здоровую долю щитовидки для того, чтобы железа смогла поддерживать нормальную выработку гормонов. В таком случае, необходимость пожизненной гормональной терапии пропадает.
Окончательное решение, о назначении или неназначении пожизненной супрессивной терапии принимается не менее чем через год после проведения основного курса лечения.
Бывает, что даже при частичном удалении щитовидки, уровень выработки гормонов падает настолько, что пациенту все равно приходится принимать синтетические препараты.
В таком случае назначается повторная операция по полному удалению щитовидной железы, для того, чтобы избежать рецидива рака в дальнейшем.
Побочные эффекты
При проведении супрессивной терапии неприятные побочные симптомы могут возникнуть лишь в том случае, если подобраны неправильные дозы гормона
Недостаточное количество препарата приведет к развитию гипотериоза. А прием слишком большого количества левотироксина приведет к тиреотоксикозу.
Регулярный прием повышенной дозы левотироксина приведет к следующим неприятным симптомам:
- тахикардия,
- частое сердцебиение,
- бессонница,
- повышенное беспокойство,
- приступы паники.
В долгосрочной перспективе избыток синтетического гормона в организме может привести к развитию болезней сердца.
Современные подходы к лечению высокодифференцированного рака щитовидной железы и осложнения супрессивной терапии левотироксином
Эндокринология: новости, мнения, обучение. 2016. № 2. С. 31-37.
Высокодифференцированный рак щитовидной железы (ВДРЩЖ) не является частой опухолью (встречаются не более чем в 1% случаев выявления злокачественных процессов у человека). Однако среди опухолей эндокринной системы он доминирует, составляя 90-95% тиреоидного рака [17]. Термин «высокодифференцированный рак щитовидной железы» объединяет гистологические типы папиллярных и фолликулярных карцином. Среди узловых образований щитовидной железы (ЩЖ) рак выявляется в 4,7-5,0% наблюдений [29]. В 2014 г. в России было зарегистрировано 10 358 (1655 мужчин, 8703 женщины) вновь выявленных больных раком щитовидной железы (РЩЖ). Средний возраст больных 53,7 года (мужчины -53,1 года, женщины — 53,9 года). Прирост абсолютного числа заболевших составил 1,88% у мужчин и 7,73% у женщин. Мужчины болели РЩЖ значительно реже женщин [2].
Отличительные особенности ВДРЩЖ — очень медленный рост и хороший прогноз при своевременном выявлении и правильно проведенном лечении. Согласно результатам исследований F.P. Ruggiero и F.G. Fedok [27], у 20% больных ВДРЩЖ развиваются рецидивы, что в 8% наблюдений приводит к неблагоприятному прогнозу. L. Duntas и соавт. [13] указывают на 30% рецидивов после 30 лет наблюдении за больными ВДРЩЖ. В исследовании J. ALbores-Saavedra и соавт. [4] 10-летняя выживаемость больных ВДРЩЖ превышает 90% [4]. Смертность 70% больных обусловлена высокодифференцированным папиллярным и фолликулярным РЩЖ [9]. По данным И.В. Комиссаренко и соавт. [3], летальность, связанная с ВДРЩЖ, у пациентов до 40 лет составляет 3,4%, от 41 до 60 лет — 6,9%, у больных старше 65 лет этот показатель увеличивается до 24,4%. J.D. Lin и соавт. [19] отмечают, что смертность у больных папиллярным РЩЖ HN0M0 составляет 19%.
По результатам многочисленных исследований, на прогноз у больных ВДРЩЖ влияет множество факторов: возраст и пол пациента, местное распространение опухоли и отдаленные метастазы, стадия опухолевого процесса, объем и методика операции, послеоперационная радиойодтерапия (РЙТ) и супрессивная терапия препаратами левотироксина (L-T4). При этом, согласно разным исследованиям, степень влияния этих факторов на прогноз у больных ВДРЩЖ кардинально отличается. Наибольшие споры вызывают объем оперативного вмешательства и тактика послеоперационного ведения больного.
Российские клинические рекомендации по диагностике и лечению высокодифференшированного рака щитовидной железы у взрослых (2016 г.) Объем хирургического лечения
Специалистами ФГБУ «Эндокринологического научного центра» Минздрава России разработан проект Российских клинических рекомендаций по диагностике и лечению ВДРЩЖ у взрослых (редакция 2016 г.) [1]. Согласно данным рекомендациям, стандартной операцией при ВДРЩЖ является экстрафасциальная тиреоидэктомия. Вмешательство такого объема снижает риск летального исхода и персистенции заболевания и сопряжено с минимальным риском осложнений при выполнении опытным хирургом. Гемитиреоидэктомия может быть выполнена при солитарной опухоли ЩЖ размером <2 см (Т1) в отсутствие достоверных до-, интра- и послеоперационных данных о поражении регионарных лимфатических узлов и отдаленных метастазах. При размере опухоли <2 см, но при наличии данных об экстракапсулярной инвазии или о предоперационном парезе голосовой связки со стороны поражения необходима тиреоидэктомия. Пациент, которому предлагают выполнить или уже выполнили гемитиреоидэктомию, должен быть предупрежден о вероятности рецидива в контрлатеральной доле и зоне регионарного лимфооттока, сложности послеоперационного стадирования заболевания и, соответственно, планировании дальнейшего наблюдения: проведение сцинтиграфии всего тела (СВТ) и оценка тиреоглобулина (ТГ). Показанием к хирургическому лечению при ВДРЩЖ являются IV-VI категории цитологического заключения по современной Международной цитологической классификации (Bethesda Thyroid Classification, 2009) (табл. 1). При III категории (атипия неясного значения) необходима повторная пункция, по результатам которой уточняется степень риска злокачественности узла. Показания к оперативному лечению при III и IV категориях цитологического заключения могут обсуждаться в индивидуальном порядке с пациентом в рамках дополнительного использования применяемых молекулярно-генетических панелей, дающих дополнительную информацию о риске ВДРЩЖ. Однако в связи с крайне ограниченным опытом таких исследований в России группа экспертов на момент публикации клинических рекомендаций не высказывается ни «за», ни «против». Первичный объем оперативного лечения при заключениях, в разной степени подозрительных в отношении ВДРЩЖ (III-V категории), зависит от тактики, принятой в конкретном специализированном учреждении. Основополагающим является определение окончательного объема оперативного лечения по результатам планового гистологического исследования [1].
Удаление лимфатических узлов центральной зоны (VI уровень) показано, если по данным дооперационного обследования есть подозрение на наличие метастазов в этой зоне или они выявлены интраоперационно. Профилактическое удаление лимфатических узлов VI зоны при размере опухоли (опухолей) <2 см увеличивает количество осложнений, не влияя на смертность, однако снижает количество рецидивов и повторных вмешательств (частота микрометастазирования в центральной клетчатке составляет 25-30%). Большинство экспертов высказываются против этой процедуры. Удаление клетчатки VII зоны показано при наличии данных предоперационой компьютерной томографии (КТ) с контрастированием о метастазировании в этой зоне.
Удаление клетчатки II-V уровней фасциально-клетчаточного пространства шеи выполняют только при доказанном метастатическом поражении по результатам тонкоигольной аспирационной биопсии (ТАБ). Первичное избирательное удаление метастатических лимфоузлов без удаления футлярно-фасциального блока не рекомендовано [1].
Послеоперационное стадирование
Определение стадии заболевания после операции необходимо для оценки индивидуального прогноза и выбора протокола дальнейшего ведения пациента [1]:
- группа низкого риска — пациенты с солитарной или первично-множественной опухолью HN0M0;
- группа промежуточного риска — пациенты с солитарной или первично-множественной опухолью Т23N01M0;
- группа высокого риска — пациенты с любой опухолью Т4N1М0, любые ТN при М1.
Послеоперационная радиойодтерапия
Терапия 131I позволяет уничтожить микроскопические остатки опухоли, а в некоторых наблюдениях оказывает полный или частичный лечебный эффект при метастазировании в легких. РЙТ в целом оказывает положительное влияние на смертность и безрецидивную выживаемость в группе промежуточного и высокого риска. РЙТ проводится на фоне безйодной диеты и высокого уровня тиреотропного гормона (ТТГ). Последний может достигаться эндогенной стимуляцией или введением рекомбинантного ТТГ. В настоящий момент не доказаны сравнительные лечебные и диагностические преимущества и недостатки каждого метода при явном преимуществе в комфорте со стороны рекомбинантного ТТГ. В настоящий момент применение рекомбинантного ТТГ определяется его труднодоступностью в Российской Федерации и требует дальнейших исследований. Радиойодтерапия 131I позволяет на 2-3-и сутки провести СВТ и выявить недиагностированные метастазы. Показания для проведения радиойодтерапии 131I определяются послеоперационным стадированием. В связи с отсутствием влияния на показатели смертности проведение РЙТ в группе низкого риска не показано. Радиойодтерапия 131I показана всем больным группы промежуточного и высокого риска, так как она достоверно уменьшает вероятность прогрессирования заболевания и увеличивает выживаемость, но может отличаться режимом дозирования [1].
Супрессивная терапия препаратами тиреоидных гормонов
Заместительная терапия препаратами тиреоидных гормонов направлена на коррекцию послеоперационного гипотиреоза, супрессивная — на подавление ТТГ-зависимого роста остаточных опухолевых клеток. Препаратом выбора является левотироксин (L-T4). Супрессивная терапия показана пациентам с доказанной опухолевой персистенцией ВДРЩЖ при отсутствии у них ишемической болезни сердца, тахиаритмий, прогрессирующего остеопороза. Целевое значение ТТГ не должно превышать 0,1 мЕд/л при нормальных значениях свободного Т4. Заместительная терапия показана пациентам с ВДРЩЖ после операции без доказанной опухолевой персистенции и любым пациентам при наличии у них ишемической болезни сердца, тахиаритмий, прогрессирующем остеопорозе. Целевое значение ТТГ — 0,2-1 мЕд/л [1].
Клинические рекомендации Европейской и Американской тиреоидных ассоциаций
Существующие европейские и американские клинические рекомендации (2006 г.) сходны с рекомендациями российских специалистов по объему хирургического лечения и показаниям к проведению РЙТ [21, 8,5]. При этом подходы к назначению супрессивной терапии различаются. Если, по мнению российских специалистов, при назначении супрессивной терапии в первую очередь необходимо учитывать наличие у пациентов заболеваний сердечно-сосудистой (ишемическая болезнь сердца, тахиаритмии) и костной (остеопороз) систем, то в клинических рекомендациях Европейской (ETA) и Американской (ATA) тиреоидных ассоциаций супрессивная терапия показана всем больным ВДРЩЖ независимо от сопутствующей патологии. Однако между этими рекомендациями существует несколько отличий в подходах к супрессивной терапии левотироксином (табл. 2).
Влияние супрессивной терапии левотироксином на сердечнососудистую систему
Терапевтический потенциал и длительность супрессивной терапии левотироксином до сих пор дискутируются. Супрессивная терапия левотироксином не безопасна для пациентов, потому что в результате ее проведения пациенты находятся в состоянии субклинического тиреотоксикоза.
В ряде исследований было доказано, что хроно-, ино- и лизинотропные (т.е. диастолическое расслабление) эффекты от избытка тиреоидных гормонов на сердце присутствуют и при субклиническом тиреотоксикозе, более того, они могут привести к повышению сердечно-сосудистой заболеваемости и смертности. У пациентов с субклиническим тиреотоксикозом при проведении 24-часового холтеровского мониторирования отмечено увеличение числа сердечных сокращений за сутки по сравнению с пациентами с эутиреозом и количества преждевременных сокращений предсердий и желудочков [7, 30]. Результаты 2 небольших исследований показали увеличение массы миокарда левого желудочка у пациентов с субклиническим тиреотоксикозом, но это наблюдение не было подтверждено в более крупных исследованиях [11, 23]. Исследования по изучению систолической и диастолической функции различными неинвазивными методами имели различные результаты: систолическая функция не была нарушена в большинстве исследований, но не во всех [24, 30, 34]. Некоторые сообщают о нарушении диастолической функции, другие исследователи не видят существенных изменений [24, 26]. Различия в возрасте пациентов, выраженности подавления ТТГ, продолжительности и причине субклинического тиреотоксикоза могут объяснить эти противоречивые результаты. В исследовании G. Leese и соавт. сравнивали обращаемость к врачу по поводу ишемической болезни сердца пациентов, получающих длительную терапию препаратами левотироксина. Оказалось, что пациенты старше 65 лет, получающие препараты левотироксина, обращались по поводу ишемической болезни сердца чаще, чем лица, не получающие подобную терапию (женщины 2,7% vs 0,7%; мужчины 6,4% vs 1,7%; р<0,01) [18].
Субклинический тиреотоксикоз может быть связан и с изменениями показателей свертывания крови [12, 14]. Некоторые подобные изменения клинически не актуальны, но сообщается о случаях тромбоза у пациентов с манифестным тиреотоксикозом, что указывает на необходимость дальнейших исследований [15]. К дополнительным факторам развития риска атеросклероза, выявленным в результате исследований, относят более выраженное увеличение комплекса интима-медиа у пациентов с субклиническим тиреотоксикозом по сравнению с пациентами в эутиреозе или «мягком» гипотиреозе [33]. К тому же при субклиническом тиреотоксикозе повышается частота образования бляшек в каротидных артериях [10].
Мерцательная аритмия при субклиническом тиреотоксикозе
Типичными аритмиями, сопровождающими субклинический тиреотоксикоз, являются мерцательная аритмия и предсердная экстрасистолия [20, 28, 32]. Тиреоидные гормоны изменяют частоту сердечных сокращений, увеличивая диастолическую деполяризацию синусового узла и облегчая проведение возбуждения через антриовентрикулярный узел. Кроме того, тиреоидные гормоны влияют на предсердные миоциты, укорачивая их рефрактерный период. Это обусловливает электрическую гетерогенность и увеличивает возможность повторной циркуляции возбуждения и предсердной фибрилляции. В условиях укорочения периода рефрактерности атриовентрикулярного узла и повышения его чувствительности к адренергической стимуляции регуляция ритма оказывается резистентной к лечению препаратами наперстянки. Желудочковые нарушения ритма встречаются редко и, как правило, у лиц с кардиальной патологией [25]. Несколько крупных исследований были посвящены оценке степени риска развития мерцания предсердия при субклиническом тиреотоксикозе. J. Auer и соавт. обследовали 23 000 человек в возрасте 6570 лет, при этом у многих имелись сердечно-сосудистые заболевания. В результате исследования установлена частота развития фибрилляции предсердий при субклиническом (13%) и манифестном тиреотоксикозе (14%) по сравнению с 2% в контрольной группе пациентов с эутиреоидным состоянием [6, 16]. В последующих исследованиях при изучении 5860 пациентов в возрасте 65 лет и старше было установлено наличие мерцательной аритмии у 5-9% пациентов с субклиническим тиреотоксикозом по сравнению с 4-7% в контрольной группе. При этом распространенность мерцательной аритмии была одинаковой как среди пациентов с уровнем ТТГ 0,1-0,4 мЕд/л, так и при ТТГ<0,1 мЕд/л [28,31].
Смертность при субклиническом тиреотоксикозе
J.V. Parle и соавт. опубликовали результаты исследования «Предсказание всех случаев смертности и смертности от сердечно-сосудистых заболеваний среди пожилых людей только на основании низкого уровня тиреотропина в сыворотке: 10-летнее когортное исследование» [22]. В данном исследовании оценивали влияние длительно существующего субклинического тиреотоксикоза на общую смертность у 1191 человека в возрасте 60 лет и старше, уровень ТТГ<0,5 мЕд/л был определен как низкий. Показано, что у пациентов с низкой концентрацией ТТГ в сыворотке наблюдалась повышенная смертность от любых причин. Причем у лиц с уровнем ТТГ<0,1 мЕд/л и 0,1-0,49 мЕд/л не отмечено разницы в выживаемости. Такая картина в значительной степени объяснялась существенным повышением уровня смертности в связи с сердечно-сосудистыми болезнями. Иными словами, низкий уровень ТТГ (<0,5 мЕд/л) ассоциируется с повышенной смертностью от всех причин, особенно от сердечно-сосудистых заболеваний. Также было отмечено отсутствие значимой взаимосвязи между сывороточными уровнями свободных T4 или T3 и смертностью у лиц с низким уровнем сывороточного ТТГ, «что свидетельствует о высокой специфичности сывороточного ТТГ как маркера функционального состояния щитовидной железы» [22].
Заключение
Согласно статическим данным, заболеваемость ВДРЩЖ неуклонно растет. В настоящее время разработаны Российские клинические рекомендации по диагностике и лечению ВДРЩЖ у взрослых, клинические рекомендации ETA и ATA. И если эти рекомендации совпадают по объему хирургического лечения в зависимости от распространенности процесса и требованиям к необходимости проведения РЙТ в послеоперационном периоде, то подходы к назначению супрессивной терапии левотироксином различаются. Сама супрессивная терапия неблагоприятно влияет на организм человека и прежде всего на сердечно-сосудистую систему, что требует дальнейшего изучения и проведения дополнительных исследований.Сведения об авторах
Татьяна Юльевна Демидова — доктор медицинских наук, профессор кафедры эндокринологии
Место работы: ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России, Москва
e-mail: [email protected]
Ирина Николаевна Дроздова — аспирант кафедры эндокринологии и диабетологии
Место работы: ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздрава России, Москва
e-mail: [email protected]
Филипп Александрович Орлов — доктор медицинских наук
Место работы: ФГКУ «Главный военный клинический госпиталь им. Н.Н. Бурденко» Минобороны России, Москва
Николай Павлович Потехин — доктор медицинских наук, профессор
Место работы: ФГКУ «Главный военный клинический госпиталь им. Н.Н. Бурденко» Минобороны России, Москва
супрессивная терапия герпеса, ответы врачей, консультация
2014-07-15 20:21:37
Спрашивает Апрель:
Здравствуйте, доктор! Помогите пожалуйста! Ситуация следующая: я забеременела на фоне супрессивной терапии валтрекс (частенько выскивал на ягодице и половых губах герпес). После наступления беременности валтрекс отменила ( 500 мг в сутки, пила около 4х месяцев).Во время беременности были рецедивы, мазала зовираксом. С 37 недели начала принимать валтрекс по 40 для предупреждения рецедива (так как я живу за границей, то борюсь с герпесом самостоятельно, врачи говорят кушайте мясо красное , пейте валтрекс при рецедивах и будет вам счастье). На 40 ой неделе бросила( не знаю зачем) и случился рецедив на ягодице. Опять начала пить валтрекс (500 мг — 2 раза в день до родов). Герпес прошел. Родила на 41 неделе. В итоге роды оказались тяжелыми — была эпизиотомия. Мне сделали эпидуральную анестезию. И теперь я мучаюсь 10 месяцев, мне ничего не помогает. Во первых, у меня периодически сумасшедшие тянущие боли в вагине, гинекологи ничего не находят и говорят попить антидепресанты. Но я уверена, что герпес перебрался на слизистую там где шов. Во вторых мне перестали помогать таблетки. Сначала я пила по 500 мг валтрекс ( супрессивная терапия 2 мес) но рецедивы не проходили . Потом выскочил огромный герпес на пол ягодицы и мне назначили бривудин. Помогло на 3 недели. Затем перешла опять на валтрекс, но уже 1000 мг в сутки, но опять тянуло все болело. Повысила дозу до 2000 мг в сутки, но все равно тянуло ягодицу, а на следующий день красное пятно ( без пузырьков). На валтрексе последние месяца 4 беспрерывно, но , видимо, он мне плохо стал помогать. Могла ли эпидуральная анестезия так повлиять на герпес??? И что делать?? Помогите!!!!
18 июля 2014 года
Отвечает Дикая Надежда Ивановна:
В лечении герпеса может помогать виферон в свечах( можно ставить ректально), неовир в инъекциях, внутривенное введение иммуноглобулина. Возможно использование вакцинотерапии, озонотерапии, плазмофореза, аутогемотерапии. К проблеме необходимо подходить комплексно, необходимо наблюдение и контроль врача иммунолога, потому, что течение герпесной инфекции часто сопровождается иммунодефицитом. Для облегчения болевого симптома возможно использование диклоберла или вольтарена в свечах, таблетках или инъекциях. Возможно использование протефлазида.
2013-03-12 17:40:28
Спрашивает Ольга:
Добрый день. Около года болею генитальным герпесом, рецидивы каждые 2 недели. Лечилась ацикловиром+ циклоферон по схеме, не супрессивной терапии рецидив, сдала анализы антитела М и G положительные, поменяли ацикловир на валтрекс, через полтора месяца приема валтрекса по 500 мг ежедневно рецидив. Очень хочу иметь ребенка, врач запрещает беременеть в связи с наличием положительного результата на антитела М. Стойкой ремиссии на фоне супрессивной терапии не наблюдается, неужели беременность не для меня?
01 апреля 2013 года
Отвечает Пурпура Роксолана Йосиповна:
Тактика врача правильная, планировать беременность можно только на фоне стойкой ремиссии. В нашей практике неплохой эффект дает Алокин альфа 6 инъекций.
2011-10-26 12:59:28
Спрашивает муся:
Здраствуйте!У моего мужа генитальний герпес,а у меня нет (здавала анализы)Рецедиви у него 2-3 раза в год,секс только защищеный и не вовремя проевления.Но всеравно мне страшно заразитса,много соримся и интим бывает редко…Я не знаю как быть дальше,ведь я его люблю,но болезнь…Скажите, пожалуста,могу ли я прожить с ним всю жизнь и не заболеть пользуясь презервативом и он принимает Вальтрекс(супрессивную терапию)?Спасибо,жду ответа!
01 ноября 2011 года
Отвечает Силко Ярослав Геннадьевич:
Здраствуйте! Конечно вы можете прожить с ним всю жизнь и не заболеть,если будете предохраняться,тем более он принимает противовирусную терапию.
2011-04-22 13:11:27
Спрашивает Елена:
Здравствуйте! У меня 2 года назад начались урогенитальные проблемы: зуд, отечность и вообще неприятные ощущения. В течении этих 2 лет часто болела ангиной и мне прописывали антибиотики. Сдала анализы ПЦР и выявилось: гарднерелла, уреаплазма. Снова прошла 3 курса подряд с антибиотиками т.к. улучшения были временные, хотя анализы повторные не высеяли ни гарднереллу ни уреаплазму. Пошла к частному гинекологу и она сказала, что это генитальный герпес. Снова пролечилась, но уже без антибиотиков. Вроде бы зажили все язвочки на слизистой, но через месяц все стало повторятся. Теперь в течении полугода каждый месяц происходят рецидивы. Прочла про супрессивную терапию. Можно ли пить ацикловир в течении года. Гинеколог говорит, что надо повышать иммунитет.
Скажите пожалуйста, как можно лечить генитальный герпес?
03 июня 2011 года
Отвечает Дикая Надежда Ивановна:
Добрый день. Лечение генитального герпеса комплексное. Необходимо лечение партнера. обычно назначаются таблетки паралельно с применением мази, свечей, примерно 7-10 дней. Вторым курсом: внутримышечно иммуноглобулины противогерпесные, два раза в неделю, №6., на фоне этого можно начать давно забытый метод- это аутогемотерапию с глюконатом кальция, вит.С. Затем курс лавомакса со свечами. Супрессивный метод можно попробовать, но он не всегда эффективен. Паралельно с противовирусными препаратами необходимо помнить, что кишечник теряет бифидум бактерии. Весь иммунитет зависит от работы кишечника. Можно попробовать электроферез плазмы крови. Извините, но недостаточно просто написать на листике лечение, нужно видить проблему, и контролировать.
2011-03-17 12:13:39
Спрашивает Лидия:
Здравствуйте, подскажите мне вот что.
Предыстория. Первичный эпизод ген герпеса был у меня в начале ноября 2010(тогда врач приняла это за стафилококк, никаких анализов и лечения не назначала), с тех пор спустя два месяца начали проявляться рецидивы, уже около 4х раз, естественно от врача я отказалась, сама сдавала анализы, герпес был обнаружен из высыпаний со второго раза методом ПЦР. IgG в крови на тип 1 и 2 — 25ДИ,через две недели 36ДИ, при норме ниже 10ДИ, IgM всегда отриц. Сдала также отдельно на 2(генитальный)тип — рез-ты 1:2 слабоположительно, через 2 недели 1:4 слабоположительно. Сдавала анализ на ТОРЧ, краснуха, хламидии, токсоплазмоз — отрицат. цитомегаловирус — 65ДИ, через 2 недели — 64ДИ, нужно ли мне обследование ПЦР на цитомегаловирус?
Партнер постоянный уже больше года.У него никаких проявлений нет и не было.Только герпес на губах часто.
В ближайшем будущем хочу планировать беременность, естественно меня волнует проблема герпеса. Собираюсь пройти супрессивную терапию Вальтрексом в течении полугода. Грамотного врача, который специализируется на лечении вирусных заболеваний я не знаю. Подскажите, какие анализы мне сдать перед планированием и как контролировать герпес во время беременности.
Заранее спасибо за ответ 🙂
17 мая 2011 года
Отвечает Консультант медицинской лаборатории «Синэво Украина»:
Добрый день, Лидия! На самом деле все очень просто. Судя по результатам анализов, Вы, как и большинство взрослых, являетесь пожизненным носителем ЦМВ и ВПГ ½. Но носительство само по себе абсолютно не опасно и лечения не требует. Лечить нужно только активную ЦМВ и герпетическую инфекцию. Соответственно, если нет активации инфекции, то ни о какой супрессивной терапии речь идти не должна. Так как избавиться от вирусов нельзя, а супрессивная терапия, если к ее проведению нет показаний, в лучшем случае не принесет вреда, в худшем, приведет к активизации вирусов. Вам всего лишь нужно регулярно контролировать активность этих вирусов. Активность вирусов нужно проверить перед зачатием, затем контролировать в каждом триместре беременности и дополнительно при появлении сыпи или симптомов ОРВИ во время нее. Для этого Вам нужно методом ПЦР проводить анализ крови (ЦМВ, ВПГ ½), мочи и слюны (ЦМВ) на ДНК вирусов. Если ДНК вирусов не обнаружена, значит, вирусы спят, вреда не причиняют, беременности не мешают, лечения не требуют. Соответственно, если ДНК вирусов обнаружена (особенно в крови), идите на очный прием к инфекционисту и под его руководством проводите адекватное противовирусное лечение. Будьте здоровы!

Читать дальше
Генитальный герпесГГ является одной из самих распространенных вирусных инфекций человека. Свыше 90% населения земного шара инфицировано ВПГ, и до 20% из них имеют те или иные клинические проявления инфекции. Герпетические инфекции представляют собой группу…
методы проведения, необходимые препараты и результаты
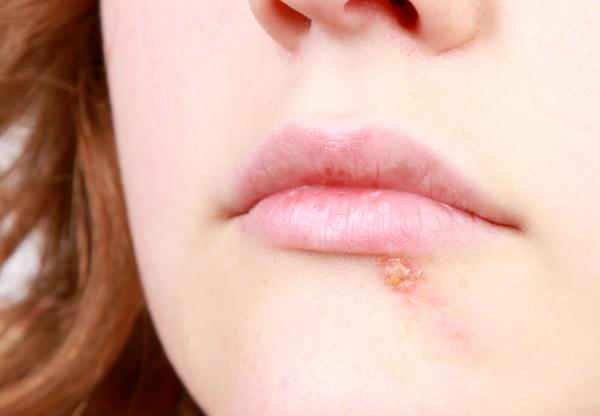
Чаще всего герпесом в народе называют высыпания на губах. На самом деле существует 8 типов этого заболевания, каждый из которых имеет свои особенности, отличительные признаки и формы лечения. Супрессивная терапия герпеса — это методика, позволяющая забыть не только о проявлениях болезни, но и о самом заболевании. На какие результаты лечения можно рассчитывать и что это такое — читайте ниже.
Подробнее о способе
Большинство людей, страдающих от вируса герпеса в крови, избавляются от его проявлений на кожном покрове в момент возникновения высыпаний. Многие специалисты говорят о более эффективном методе борьбы с неприятными симптомами. Супрессивная терапия герпеса — это способ лечения, при котором лекарственные препараты принимаются постоянно, подавляя сам вирус и не допуская возникновения его симптомов. Данный метод требует от больного особого внимания к принимаемым средствам и самому курсу лечения. Ведь если перестать употреблять лекарства после исчезновения неприятных признаков, необходимого положительного эффекта не будет. Помимо этого, после прекращения использования медикаментов герпес может проявиться еще сильнее. Но при правильном соблюдении схемы приема лекарственных препаратов о заболевании можно забыть насовсем.
Плюсы лечения
У пациента всегда есть выбор: можно использовать противовирусную терапию против герпеса только во время обострения заболевания или же получить супрессивное лечение (прием медикаментов в течение года). Преимущество последнего заключается в следующем:
- В некоторых случаях после его проведения происходит полное выздоровление.
- При длительном приеме лекарственных препаратов обострения протекают легче: меньше беспокоят зуд и боль, а сам период обострения значительно сокращается.
- Больные герпесом могут заразить окружающих. Даже во время ремиссии можно передать партнеру вирус во время секса. При проведении супрессивной терапии вероятность такого заражения уменьшается.
- Живущие в человеке патогенные микроорганизмы негативно воздействует на иммунную систему. При проведении длительного противогерпетического лечения отрицательное действие вируса на иммунитет снижается, а защитные силы организма страдают меньше.
Основные эффекты
Что же может дать супрессивная терапия герпеса:
- Контроль над течением болезни.
- Уменьшение выделения вируса и возможности заражения других людей.
- Улучшение качества жизни.
- Полное уничтожение вируса. Стоит отметить, что такое происходит редко и только в том случае, когда герпес-терапия началась при первой атаке вируса (в первые 24 часа), когда он еще не успел перейти в латентное состояние.
После проведения терапии в течение одного года специалисты рекомендуют сделать небольшой перерыв (не менее двух месяцев) и оценить эффективность метода. При необходимости дополнительно к препаратам против герпеса назначаются витаминно-минеральный комплекс и иммуномодуляторы.
Минусы терапии

Поскольку супрессивное лечение предусматривает долгий прием лекарственных препаратов, такая терапия имеет и негативные стороны. Во время прохождения курса пациент может жаловаться на тошноту и рвоту, вздутие или боли в животе.
В редких случаях проявляется диффузная алопеция (облысение) и кожные высыпания. Лекарство может не подходить больному. В таких случаях человек может испытывать сонливость, заторможенность, отмечать скованность мышц, боль в них, аллергический насморк. В тяжелых случаях возможны даже удушье и анафилактический шок, судороги.
Беременность и супрессивная терапия герпеса несовместимы. Препараты не назначают во время вынашивания плода и в период лактации, так как компоненты, входящие в состав лекарств, могут через кровь и молоко передаваться малышу. А из-за несформированной иммунной системы лекарства не назначают детям до трехлетнего возраста, так как они могут принести больше вреда, чем пользы.
Стоит знать, что при прохождении курса супрессивной терапии вирус может показать себя активными высыпаниями. Это считается нормальной реакцией на лечение, а частота обострений постепенно будет снижаться, и они полностью сойдут на нет.
Действие лекарственных средств

Супрессивная терапия генитального герпеса, а также других видов заболевания рекомендуется в том случае, если болезнь проявляется пять и более раз в год. При обострении заболевания менее 5 раз в год длительное лечение не назначают. В таком случае противовирусные препараты выписывают только в период обострения. Как правило, длительное лечение назначают на срок один год, оно включает в себя ежедневный прием следующих препаратов:
- «Ацикловир».
- «Фамцикловир».
- «Валацикловир».
В аптеках можно встретить много аналогов этих средств. Каждый производитель по-своему называет такой препарат.
«Фамцикловир» и «Валацикловир» являются неактивными соединениями, которые при попадании в организм человека преобразовываются в пенцикловир и ацикловир. Механизм действия этих препаратов основан на подавление у делящихся вирусов герпеса клеток ДНК.
В вирусную клетку встраивается производный элемент от ацикловира. Такая ДНК уже не может воспроизводить новые вирусные клетки. Современные препараты против герпеса не воздействуют на клетки, пораженные вирусом, которые находятся в спящем состоянии. Поэтому полное излечение от заболевания практически невозможно.
В редких случаях встречается невосприимчивость вируса к лечебным препаратам. Такое случается у ВИЧ-инфицированных и у лиц, длительно проходивших супрессивную терапию. Чаще всего переносимость медикаментов хорошая. Данные лекарства не обладают мутагенным и тератогенным воздействиями. Разрешается комбинированный прием противогерпетических средств с препаратами из других фармакологических групп.
Данные лекарства не подавляют кишечную микрофлору. Помимо этого, они не оказывают негативного влияния на почки и печень. После приема противогерпетических препаратов главное действующее вещество попадает в клетки и быстро всасывается, начиная воздействие на ДНК вируса. Стоит отметить, что в некоторых ситуациях супрессивную терапию герпеса могут назначить беременной женщине. Это происходит только в тех случаях, когда ожидаемая польза выше, чем возможный риск для ребенка.
Отличительные черты лекарств

Каждый из представленных медикаментов отличается своим механизмом действия и свойствами:
- Супрессивная терапия герпеса «Ацикловиром» эффективна при первой атаке вируса.
- «Валацикловир» менее токсичен, чем «Ацикловир» и его аналоги. Он позволяет добиться необходимой концентрации ацикловира в клетках при меньшей дозировке. Данный препарат противопоказан лицам до 18 лет. Терапия герпеса «Валацикловиром» считается более эффективной, чем «Ацикловиром».
- «Фамцикловир». Это самый дорогой препарат. Он эффективен при иммунодефиците. Его выписывают при тяжелых формах герпетической инфекции.
Цена
Самым дешевым из вышеперечисленных средств является «Ацикловир». «Валацикловир» обойдется немного дороже. Курс «Фамцикловира», рассчитанный на год лечения, будет стоить примерно 6000 долларов. Каждый больной выбирает препарат, доступный ему по цене. Более низкая стоимость средства не означает, что оно менее эффективно. Скорее, оно просто отечественного изготовления. А зарубежные лекарства всегда дороже, ведь в стоимость такого препарата входит цена за перевозку.
Сравнительная характеристика препаратов
Выбирая препарат для супрессивной терапии герпеса, необходимо обратить внимание на преимущества и недостатки.
Преимущества «Ацикловира»:
- Низкая цена.
- Назначается детям.
- Мало побочных эффектов.
- Хорошо изучен.
- В некоторых случаях назначается при беременности.
Недостатком является низкая биодоступность. Для достижения необходимой концентрации средства в клетках нужна большая доза препарата.
Преимущества «Валацикловира»:
- Всасываемость лекарства не зависит от приема пищи.
- Высокая биодоступность (для получения нужного эффекта требуется небольшая доза).
- Меньшая частота приема во время курса.
К недостаткам «Валацикловира» можно отнести дороговизну.
Преимущества «Фамцикловира»:
- Всасываемость препарата не зависит от приема пищи.
- Действует только на зараженные клетки.
- Воздействует на вирусы, которые имеют устойчивость к «Ацикловиру».
- Высокая биодоступность.
Недостатком препарата является высокая цена.
Каждый пациент может подобрать медикаменты для лечения, основываясь на своих предпочтениях, согласно таким параметрам: зависимость от приема пищи, стоимость, частота приема, побочные эффекты. Следует понимать, что самолечением заниматься не стоит. Терапевтический курс должен назначать специалист, который порекомендует наиболее эффективное лекарство в каждом конкретном случае.
Дополнение к лечению
Сразу после супрессивной терапии обострение герпеса может произойти на фоне снижения защитных сил организма. Именно поэтому в дополнение к лечению часто назначают иммуномодуляторы. Некоторые врачи не согласны с этим, особенно если иммуномодуляторы прописываются без предварительной иммунограммы.
В некоторых случаях для снижения числа рецидивов и улучшения общего состояния больного может быть полезен витаминно-минеральный и антиоксидантный комплекс. В аптеках можно найти несколько препаратов, которые содержат в себе все необходимые полезные вещества.
Что говорят пациенты

На различных форумах и в тематических сообществах можно встретить много отзывов о супрессивной терапии герпеса. Говорить о стопроцентной эффективности данного метода невозможно. Ведь известно, что каждый организм индивидуален. Кому-то такое лечение приносит ощутимый результат, а кто-то месяцами перебирает различные препараты, для того чтобы найти подходящий. Абсолютно всем больным лечение назначается лечащим врачом. Многие пациенты жалуются на частые обострения на начальном этапе приема препаратов. Специалисты утверждают, что такое явление считается нормой, и со временем негативные симптомы проявляются намного реже. Самым популярным препаратом является «Ацикловир». Это связано с эффективностью и низкой стоимостью средства.
Заключение
Длительная противовирусная терапия герпеса является эффективным методом лечения только в тех случаях, когда вирус дает о себе знать более пяти раз в год. Не рекомендуется самостоятельно подбирать лекарственный препарат. Только специалист после проведения диагностических исследований может назначить подходящее лекарство.


Добавить комментарий