Аутофагия — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 23 октября 2019; проверки требуют 16 правок. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 23 октября 2019; проверки требуют 16 правок.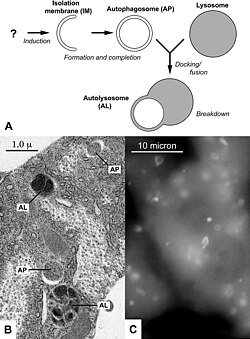 A: Схема образования аутофагосомы: изолирующая мембрана окружает клеточные структуры и создает аутофагосому (AP), которая сливается с лизосомой и создает аутолизосому (AL). B: Электронная микрофотография аутофагосомных структур в жировом теле личинки дрозофилы. С: Помеченные флуоресцентной меткой аутофагосомы в клетках печени голодающей мыши
A: Схема образования аутофагосомы: изолирующая мембрана окружает клеточные структуры и создает аутофагосому (AP), которая сливается с лизосомой и создает аутолизосому (AL). B: Электронная микрофотография аутофагосомных структур в жировом теле личинки дрозофилы. С: Помеченные флуоресцентной меткой аутофагосомы в клетках печени голодающей мышиАутофагия (от др.-греч. αὐτός ауто- — сам и φαγεῖν — «есть») — является естественным, регулируемым механизмом клетки, который разбирает ненужные или дисфункциональные компоненты
Сейчас различают три типа аутофагии — микроаутофагию, макроаутофагию и шапероновую аутофагию.
При микроаутофагии макромолекулы и обломки клеточных мембран просто захватываются лизосомой. Таким путём клетка может переваривать белки при нехватке энергии или строительного материала (например, при голодании). Но процессы микроаутофагии происходят и при нормальных условиях и в целом неизбирательны. Иногда в ходе микроаутофагии перевариваются и органоиды; так, у дрожжей описана микроаутофагия пероксисом и частичная микроаутофагия ядер, при которой клетка сохраняет жизнеспособность[4].
При макроаутофагии участок цитоплазмы (часто содержащий какие-либо органоиды) окружается мембранным компартментом, похожим на цистерну эндоплазматической сети. В результате этот участок отделяется от остальной цитоплазмы двумя мембранами. Такие двухмембранные органеллы, окружающие удаляемые органеллы и цитоплазму, называются аутофагосомы. Аутофагосомы соединяются с лизосомами, образуя аутофаголизосомы, в которых органеллы и остальное содержимое аутофагосом перевариваются. Видимо, макроаутофагия также неизбирательна, хотя часто подчеркивается, что с помощью неё клетка может избавляться от «отслуживших свой срок» органоидов (митохондрий, рибосом и др.).
Третий тип аутофагии — шапероновая. При этом способе происходит направленный транспорт частично денатурировавших белков из цитоплазмы сквозь мембрану лизосомы в её полость, где они перевариваются. Этот тип аутофагии, описанный только для млекопитающих, индуцируется стрессом (например, при том-же голодании или физических нагрузках). Она происходит при участии цитоплазматических белков-шаперонов семейства hsp-70, вспомогательных белков и LAMP-2, который служит мембранным рецептором комплекса шаперона и белка, подлежащего транспорту в лизосому.
При аутофагическом типе клеточной гибели перевариваются все органеллы клетки, оставляя лишь клеточный дебрис, поглощаемый макрофагами.
Аутофагия сопровождает жизнедеятельность любой нормальной клетки в обычных условиях.
Основными стимулами к усилению процессов аутофагии в клетках могут служить:
- нехватка питательных веществ
- наличие в цитоплазме повреждённых органелл
- наличие в цитоплазме частично денатурировавших белков и их агрегатов
Кроме голодания, аутофагия может индуцироваться окислительным или токсическим стрессом. В настоящее время на дрожжах детально изучаются генетические механизмы, регулирующие аутофагию. Так, для образования аутофагосом необходима активность многочисленных белков Atg-семейства (autophagosome-related proteins). Гомологи этих белков найдены у млекопитающих (в том числе и человека) и растений.
Значение аутофагии при нормальных и патологических процессах[править | править код]
Аутофагия — один из способов избавления клеток от ненужных органелл, а также и организма от ненужных клеток. Особенно важна аутофагия в процессе эмбриогенеза, при так называемой самопрограммируемой клеточной гибели. Сейчас этот вариант аутофагии чаще называют каспаза-независимым апоптозом. Если эти процессы нарушаются, а разрушенные клетки не удаляются, то эмбрион чаще всего становится нежизнеспособным.
Иногда благодаря аутофагии клетка может восполнить недостаток питательных веществ и энергии и вернуться к нормальной жизнедеятельности. Напротив, в случае интенсификации процессов аутофагии клетки разрушаются, а их место во многих случаях занимает соединительная ткань. Подобные нарушения являются одной из причин развития сердечной недостаточности. Нарушения в процессе аутофагии могут приводить к воспалительным процессам, если части мёртвых клеток не удаляются.
Особенно большую (хотя и не до конца понятную) роль нарушения аутофагии играют в развитии миопатий и нейродегенеративных болезней. Так, при болезни Альцгеймера в отростках нейронов пораженных участков мозга наблюдается накопление незрелых аутофагосом, которые не транспортируются к телу клетки и не сливаются с лизосомами. Мутантные хантингтин и альфа-синуклеин — белки, накопление которых в нейронах вызывает, соответственно, болезнь Хантингтона и болезнь Паркинсона — поглощаются и перевариваются при шапероновой аутофагии, и активация этого процесса предотвращает образование их агрегатов в нейронах
определение, функции и виды аутофагии

 Слово «аутофагия» происходит от греческих слов «auto» и «phagy», означающих «себя» и «есть»
Слово «аутофагия» происходит от греческих слов «auto» и «phagy», означающих «себя» и «есть»Аутофагия (или аутофагоцитоз) — это адаптационный механизм клетки, позволяющий переваривать собственные компоненты, чтобы повторно использовать их материал. Адаптация может противостоять широкому спектру неблагоприятных условий, в том числе гипогликемии, гипоксии, дефициту незаменимых аминокислот или факторов роста.
Содержание:
При недостатке питательных веществ или факторов роста возникает клеточный стресс, который приводит к усилению аутофагии. Таким образом, обеспечивается альтернативный источник внутриклеточных строительных блоков и субстратов, а также энергия для обеспечения непрерывного выживания клеток.
Этот процесс наблюдается во всех эукариотических системах, включая грибы, растения, плесень, нематод, насекомых, грызунов и других млекопитающих.
Аутофагия и гибель клеток
Аутофагия позволяет клеткам не только переживать стресс из внешней среды, но также противостоит внутренним стрессам, таким как накопление поврежденных органелл и проникновение патогенов или инфекционных организмов.
При определенных условиях аутофагия может убить клетку. Это относят к второму типу запрограммированной гибели клеток (ПКГ), называемым «аутофагической гибелью клеток». Другие виды запрограммированной гибели клеток включают апоптоз и некроз.
Далеко не все согласны с тем, что аутофагия может быть нацелена на смерть клетки. Есть множество исследований, которые говорят, что она является защитным механизмом, направленным на спасение клетки.
Однако этот процесс «спасения» часто ведет к аутофагической гибели клетки, когда все ее содержимое переваривается и остается лишь клеточный дебрис, который поглощают макрофаги.
Виды аутофагии
Существует несколько видов аутофагии, каждый из которых имеет свои особенности:
- Микроаутофагия. В этом процессе цитозольные компоненты непосредственно поглощаются самой лизосомой через лизосомальную мембрану. Это позволяет клетке переваривать белки при нехватке материала или энергии (например, при голодании)
- Макроаутофагия включает отделение участка клетки двойным мембраносвязанным пузырьком (аутофагосома), в котором содержатся удаляемые органеллы и цитоплазма. Этот пузырек сливается с лизосомой, образуя аутофаголизосому, где происходит переваривание органелл и остального содержимого
- Шапероновая аутофагия. В этом процессе целевые белки перемещаются из цитоплазмы в лизосому. Процесс проходит при участии шапероновых белков (таких как Hsc-70) и гликопротеина LAMP-2
- Митофагия — это избирательная деградация митохондрий. Митофагия предотвращает накопление дисфункциональных митохондрий, которые могут привести к клеточной дегенерации, а также способствует их обновлению
- Липофагия — это деградация липидов аутофагией. Мишенью являются липидные структуры, называемые липидными каплями (LDs). Липидные капли — это сферические «органеллы» с ядром, состоящим в основном из триацилглицеринов (TAG) и однослойных фосфолипидов и мембранных белков

 Этапы макроаутофагии
Этапы макроаутофагииТермин «аутофагия» обычно обозначает макроаутофагию, если не указано иное.
Что вызывает аутофагию
Аутофагия состоит из нескольких последовательных этапов:
- Секвестрация
- Деградация
- Генерация аминокислот и пептидов.
На каждом этапе, выполняются определённые функции, в зависимости от обстоятельств. Это делает аутофагию многофункциональной.
Наиболее типичным спусковым механизмом, вызывающим аутофагию, является голодание клетки, при котором обнаруживается недостаток какого-либо питательного вещества. Например, у дрожжей, наиболее мощным стимулом служит азотное голодание, но и нехватка других важных веществ, таких как углерод, ауксотрофные аминокислоты, нуклеиновые кислоты, тоже может вызвать аутофагию, хотя и менее эффективно (Takeshige et al. 1992). Азотное или углеродное голодание также вызывает аутофагию в растительных клетках.
У млекопитающих процесс аутофагии довольно сложен. Истощение общих аминокислот сильно индуцирует аутофагию во многих типах культивируемых клеток, но эффекты отдельных аминокислот различаются. Leu, Tyr, Phe, Gln, Pro, His, Trp, Met и Ala подавляют аутофагию в перфузированной печени ex vivo (Mortimore and Poso 1987). Однако есть зависимость от типа клеток, поскольку метаболизм аминокислот сильно различается в разных тканях. Например, лейцин оказывает доминирующее влияние на скелетные мышцы и сердце.
На сегодняшний день не выявлено, как именно клетки чувствуют концентрацию аминокислот. Одним из сенсоров-кандидатов является GCN2 тРНК-связывающая протеинкиназа, а также другие аминокислотные сигнальные пути, включающие фосфатидилинозитол-3-киназу (PI3) и Beclin 1.
Считается, что сигналы аминокислот, инсулина и факторов роста сходятся на mTOR (мишень рапамицина), который является основным регулятором передачи сигналов питательных веществ. Действительно, лечение ингибиторами TOR, такими как рапамицин и CCI-779, вызывает аутофагию у дрожжей (Noda и Ohsumi 1998) и животных (Ravikumar et al. 2004). Однако не все сигналы аутофагии передаются через mTOR, некоторые аминокислотные сигналы могут подавлять аутофагию mTOR-независимым образом (Mordier et al. 2000 и Kanazawa et al. 2004).
Селективность аутофагии
Аутофагию обычно считают неселективной системой деградации. Эта особенность резко контрастирует с системой убиквитин-протеасома, которая специфически распознает только убиквитинированные белки для протеасомной деградации. Убиквитин-протеасома имеет множество специфических функций, поскольку она может избирательно разрушать тысячи субстратов.
При нормальных условиях и в течение очень коротких периодов голодания, поддержание аминокислотного пула, по-видимому, зависит главным образом от системы убиквитин-протеасома, а не от аутофагии (Vabulas и Hartl 2005). Однако во время голодания, которое продолжается в течение нескольких часов, необходимые аминокислоты вырабатываются за счет аутофагии, которая активируется как адаптивный ответ.
Аутофагия — что это такое и как она может продлить жизнь
Аутофагия – это процесс, посредством которого наши клетки перерабатывают свои компоненты. Большую часть времени аутофагия проходит спокойно в фоновом режиме, но когда клетки находятся под негативным воздействием, аутофагия становится более важной. Читайте дальше в статье, чтобы больше узнать об аутофагии и том, как она работает, что может регулировать аутофагию и какие факторы ее усиливают.
Статья основана на выводах 91 научного исследования
В статье цитируются такие авторы, как:
- Комитет по биологии рака, центр интегративных наук Гордона, Чикагский университет, Иллинойс, США
- Кафедра молекулярной биологии и биохимии, Университет Рутгерса, Пискатауэй, Нью-Джерси, США
- Молекулярно-клеточная биология аутофагии, институт Фрэнсиса Крика, Лондон, Великобритания
- Отделение биохимии и молекулярной и структурной биологии, институт Йожефа Стефана, Любляна, Словения
Обратите внимание, что цифры в скобках (1, 2, 3 и т.д.) являются кликабельными ссылками на рецензируемые научные исследования. Вы можете перейти по этим ссылкам и ознакомиться с первоисточником информации для статьи.
Что такое аутофагия?
Аутофагия (от греч. αὐτός – сам и φαγεῖν – есть) – это регулируемый процесс, посредством которого клетка разлагает свои или чужеродные компоненты. Затем клетка может перерабатывать полученные полезные химические компоненты для своего существования. (1)
Это позволяет аутофагии регулировать баланс белкового состава в клетке, предотвращать накопление токсичных отходов, поддерживать функцию клеточных органелл, удалять вторгающиеся патогены и поддерживать клетки в периоды низких энергозатрат при голоде. (2)
Научное понимание аутофагии было подчеркнуто, когда японский ученый Есинори Осуми получил Нобелевскую премию по физиологии и медицине за свои открытия механизмов аутофагии в 2016 году.
 ЕСИНОРИ ОСУМИ ПОЛУЧИЛ В 2016 ГОДУ НОБЕЛЕВСКУЮ ПРЕМИЮ ЗА ОТКРЫТИЕ МЕХАНИЗМА АУТОФАГИИ
ЕСИНОРИ ОСУМИ ПОЛУЧИЛ В 2016 ГОДУ НОБЕЛЕВСКУЮ ПРЕМИЮ ЗА ОТКРЫТИЕ МЕХАНИЗМА АУТОФАГИИМеханизм аутофагии
По существу аутофагия – это создание “мусорного мешка” (аутофагосомы), в который собираются клеточные компоненты и затем они доставляются в “центр рециркуляции” клетки (лизосому), чтобы разбить их на составные молекулы, которые затем могут быть переработаны в новые компоненты клетки.
Гены связанные с аутофагией отвечают за производство структур, осуществляющих аутофагию. Комплекс VPS34 (PI 3-киназа III класса) инициирует аутофагосому, ген ATG9 способствует ее расширению, а комплекс генов ATG12 – ATG5– ATG16L1 рекрутирует белки ATG8, которые завершают образование и участвуют в целенаправленном захвате составных молекул. (3)
Другие гены участвуют во включении и выключении аутофагии. Эти гены могут обнаруживать негативные изменения в клетке. Протеинкиназа mTOR реагирует на уровень питательных веществ в клетке и уменьшает аутофагию (разрушая ULK1, предотвращая образование комплекса VPS 34), когда у клетки есть много доступных питательных веществ. Клеточная протеинкиназа АМФК контролирует энергетические уровни в клетке (количество АТФ) и активирует аутофагию, когда это количество снижается. Ген HIF1A обнаруживает доступное количество кислорода и включает аутофагию (нацеливание митохондрий), когда уровень кислорода снижается (гипоксия). (4, 5)
Недавнее исследование выявило, что белок p62 (белковый комплекс, связанный с ядерной оболочкой) помогает доставлять различные типы мусора в клеточные “перерабатывающие центры” и при его сильной и длительной активации приводит к 20-30% увеличению длительности жизни короткоживущих прозрачных круглых червей. Белок p62 является драйвером процесса переработки в процессе аутофагии. Известно, что p62 избирательно доставляет агрегированные белки и изношенные митохондрии в центры рециркуляции. (90)
 СХЕМА АУТОФАГИИ
СХЕМА АУТОФАГИИГены сиртуина (активируемые ресвератролом) могут ингибировать mTOR, что повышает аутофагию. (6) Сообщается также, что низкие уровни кофермента NAD+ (никотинамидадениндинуклеоти́да) увеличивают аутофагию. (7)
Ограничения исследований аутофагии
К сожалению, механизмы аутофагии чрезвычайно трудно изучить у человека, поэтому подавляющее большинство исследований, обсуждаемых в этой статье, было проведено на животных и клетках. Такое отсутствие клинических доказательств означает, что очень мало достоверных выводов можно сделать об аутофагии и её связи со здоровьем человека.
Цели аутофагии
Когда все идет гладко в клетке, процесс аутофагии находится на низком уровне, помогая перерабатывать изношенные клеточные компоненты. Это своего рода режим “технического обслуживания” наших клеток.
Но когда в клетке возникает стресс (недостаточно питательных веществ или энергии, увеличивается количество измененных компонентов или происходит вторжение микробов), то аутофагия включается на полную мощность, чтобы помочь защитить нас. Этот режим аутофагии называется – “реакция на стресс”.
Старение и продолжительность жизни
Активация аутофагии противодействует возрастному накоплению поврежденных клеточных компонентов и повышает метаболическую эффективность клеток. (8)
Аутофагия – это ответ на стресс, что помогает клеткам стать более устойчивыми при снижении доступной энергии. В частности, аутофагия может быть активирована для удаления дисфункциональных митохондрий (митофагия), которые производят много вредных активных форм кислорода(АФК), приводящих к деградации клетки. (9) Эти процессы, как сообщается наукой, увеличивают продолжительность жизни нескольких видов животных.
Психический стресс
Типичное действие аутофагии обеспечивает защиту от развития психических расстройств. Нарушения аутофагических процессов связаны с повышенным риском развития некоторых психических заболеваний, в том числе, депрессии и шизофрении. (11)
Посмертные исследования головного мозга людей с депрессией и шизофренией выявили недостаточность основных аутофагических путей. (12, 13)
Нейродегенерация
Многие нейродегенеративные заболевания проистекают из накопления деформированных белков в нейронах и вокруг них, вызывая постепенную гибель клеток головного мозга и последующую потерю психических способностей. (14)
Аутофагия защищает нас нейродегенеративных болезней, удаляя эти белки. При болезни Хантингтона она удаляет белок хантингтона (HTT) (15), при болезни Альцгеймера она удаляет амилоид-бетта (созданный из белка APP) (16), при болезни Паркинсона она удаляет ⍺-синуклеин (SNCA), а при деменции она удаляет микротрубочко-ассоциированный белок tau. (17)
Инфекционные заболевания
Аутофагия способствует борьбе с инфекционными заболеваниями тремя способами:
- Прямое удаление микробов из клеток (ксенофаги)
- Удаление токсинов, вызванных инфекциями
- Модуляция иммунного ответа на инфекции (14)
Инфекционные микробы (такие как Mycobacterium tuberculosis s и группа бактерий Streptococcus), вирусы, такие как ВИЧ, и простейшие, удаляются из организма с помощью процессов аутофагии. (18, 19, 20, 21)
Воспаление
Аутофагия может как увеличивать, так и уменьшать воспалительные реакции в организме. Она усиливает воспаление при обнаружении инвазии патогена в клетку и стимулирует включение иммунного ответа. (22)
Аутофагия затем уменьшает воспаление, вызванное иммунным ответом, очищая клетку от антигенов, которые стимулируют этот иммунный ответ. Кроме того, аутофагия также удаляет молекулы про-иммунного ответа, продуцируемые клеткой в ответ на инвазию патогенов. (23)
 ПРОЦЕСС АУТОФАГИИ КАК СТИМУЛЯТОРА ДОЛГОЛЕТИЯ (источник)
ПРОЦЕСС АУТОФАГИИ КАК СТИМУЛЯТОРА ДОЛГОЛЕТИЯ (источник)Производительность работы мышц
Во время физической тренировки мы переносим биологический стресс на наши клетки. Потребление клеткой энергии растет, и клеточные компоненты могут изнашиваться быстрее.
При физической нагрузке аутофагия увеличивается, чтобы:
- Поддерживать баланс потребления энергии внутри клетки
- Уменьшать количество требуемой внешней энергии (более эффективно перерабатывать существующие молекулы в энергию)
- Убедиться, что деградированные клеточные компоненты удалены, прежде чем они начнут вызывать какие-либо проблемы в клетке. (24)
Рак
Аутофагия играет определенную роль в предотвращении возникновения рака и подавлении злокачественных клеток на ранних стадиях рака. Аутофагия подавляет про-раковые процессы, такие как хроническое воспаление, ответ на повреждение ДНК и нестабильность генома. (2)
Сообщается, что мыши, генетически модифицированные для нарушения аутофагии, демонстрируют повышенные риски развития рака. (25)
К сожалению, защитные функции аутофагии могут быть нарушены уже имеющимися опухолями. По мере роста опухоли серединные клетки изолируются от кровоснабжения и начинают подвергаться питательному и энергетическому стрессу. Активация аутофагии может обеспечить поддержку жизнедеятельности этих раковых клеток. Тем не менее, аутофагия, по-видимому, в целом полезна до того, чтобы сдерживать развитие раковых клеток. (26)
Что может вызвать аутофагию
Аутофагия – это важнейший клеточный процесс, который активируется, когда клетки находятся в состоянии стресса. Таким образом, мягкий стресс может быть полезным, если он активируют аутофагию, не нанося значительного ущерба самим клеткам. (27)
Кроме того, некоторые вещества в пище или пищевых добавках могут активировать механизмы аутофагии.
Обратите внимание, что взаимосвязь между аутофагией и образом жизни или диетой очень трудно продемонстрировать у людей. Таким образом, доказательства многих таких связей ограничены исследованиями на животных или клетках, что делает невозможным точно сказать, увеличат ли эти факторы аутофагию у людей, или нет.
Соблюдайте осторожность и проконсультируйтесь с врачом перед началом приема любого нового вещества, сменой режима физических упражнений или изменения образа жизни.
Слабые стрессоры которые могут вызвать аутофагию:
Другие факторы, которые могут вызвать аутофагию:
- Диетические продукты питания
- Растительные лекарственные средства
- Биологические активные добавки (БАД)
- Активные растительные соединения
- Лекарства для лечения рака
Факторы образа жизни
Аэробные физические упражнения
Было продемонстрировано, что аэробные физические упражнения индуцируют аутофагию в мышечных тканях и головном мозге у животных, вероятно, из-за длительного стресса, связанного с физической нагрузкой. (28)
Мало того, что физические упражнения заставляют вас чувствовать себя лучше и сохранять свое здоровье, но они также активируют аутофагию, чтобы гарантировать, что ваши клетки полностью восстановятся после этого стрессового процесса.
Периодическое голодание и ограничение калорийности питания
Периодическое голодание и ограничение калорий пищи активировали аутофагию у животных. (29)
Недостаток питательных веществ активирует аутофагию для увеличения переработки уже имеющихся клеточных компонентов, гарантируя, что клетки продолжат нормально функционировать при меньших требованиях к внешним ресурсам. (29)
 ОГРАНИЧЕНИЕ 8-10 ЧАСОВЫМ ИНТЕРВАЛОМ ПРИЕМ ПИЩИ В ТЕЧЕНИЕ ДНЯ – СПОСОБСТВУЕТ УСИЛЕНИЮ АУТОФАГИИ. НАПРИМЕР, ЗАВТРАК – В 8.00 УТРА И УЖИН В 18.00 ВЕЧЕРА.
ОГРАНИЧЕНИЕ 8-10 ЧАСОВЫМ ИНТЕРВАЛОМ ПРИЕМ ПИЩИ В ТЕЧЕНИЕ ДНЯ – СПОСОБСТВУЕТ УСИЛЕНИЮ АУТОФАГИИ. НАПРИМЕР, ЗАВТРАК – В 8.00 УТРА И УЖИН В 18.00 ВЕЧЕРА.Это может быть достигнуто либо путем перехода на временной интервал без еды (голодание), либо путем уменьшения количества пищи, которую вы едите (ограничение калорийности). Было продемонстрировано, что кратковременное голодание индуцирует глубокую нейрональную аутофагию и может быть хорошим методом для борьбы с неврологическими заболеваниями. (30)
Кетогенная диета
Кетогенная диета снижает потребление углеводов и увеличивает потребление жиров, что приводит к сдвигу потребления энергии с глюкозы на кетоны. Этот сдвиг имитирует процесс, который происходит во время голодания и таким образом может привести к увеличению аутофагии. (31)
Согласно исследованиям на животных, кетогенные диеты могут способствовать аутофагии в головном мозге, и некоторые ученые предположили, что такие диеты являются жизненно важным механизмом для предотвращения нейродегенеративных заболеваний. Однако эта связь не была продемонстрирована на людях. (32)
Сон
Аутофагия активируется во время сна. Циркадный ритм не только помогает контролировать ваш цикл сна, но он также связан с аутофагией. Внутренние биологические часы влияют на ритм аутофагии. (33)
У мышей нарушение сна отрицательно сказываются на аутофагии. Когда сон животных был нарушен, то последовало прерывание передачи белков аутофагии. (34)
Продукты питания
Кофе
Было продемонстрировано, что кофе увеличивает аутофагию у мышей. (35)
Большой мета-анализ исследований с участием более 340 000 человек в Англии показал, что только у тех людей, кто пил много кофе (более 6 чашек в день), частота сердечно-сосудистых заболеваний была выше, чем у тех, кто совсем не пьет кофе, в то время как умеренное потребление кофе (1-2 чашки в день) уменьшало частоту развития сердечно-сосудистых заболеваний. (36)
Хотя это исследование не изучало аутофагию специально, оно демонстрирует, что умеренное употребление кофе, по крайней мере, не вредно для сердца. Кроме того, нарушенные гены и механизмы аутофагии были связаны с повышенными рисками сердечно-сосудистых заболеваний у животных. (36, 37)
Никакие исследования не изучали, существует ли связь между кофеином, аутофагией и сердечно-сосудистыми проблемами у людей.
Зеленый чай и вещество в нем – EGCG
Согласно исследованиям на мышах, активные ингредиенты зеленого чая могут активировать аутофагию. В частности, полифенолы, такие как эпигаллокатехин-3-галлат (EGCG), активировали аутофагию в печени мышей, получавших 3,2 гр. EGCG на 1 кг их пищи. Ученые остановились на этой дозе как грубом эквиваленте для человека, выпивающему 10 чашек зеленого чая в день. (38)
Люди должны пить много зеленого чая, чтобы достичь такого потребления EGCG, и связь между EGCG и аутофагией печени не была продемонстрирована у людей.
Биологические вещества
Ресвератрол
Ресвератрол – это полифенол, содержащийся в низких дозировках в винограде, вине, арахисе и сое. (39)
В ряде исследований сообщалось об индуцирующей активности ресвератрола для запуска аутофагии в клетках. (40, 41)
У крыс ограничение калорий и прием ресвератрола (но не только он один) способствовали аутофагии в сердечной мышце. Однако это преимущество не было продемонстрировано на людях, и ресвератрол печально известен своей низкой биодоступностью. (42)
Куркумин из куркумы
Куркумин является наиболее активным фитохимическим веществом в куркуме и имеет много преимуществ для здоровья. (43) В исследовании на мышах куркумин активировал аутофагию и обратил вспять некоторые повреждения, вызванные остеоартрозом. (44)
Сообщается, что в исследованиях на клетках аутофагия активируется куркумином (через сигнальный путь AMPK). (45)
 КУРКУМИН СПОСОБСТВУЕТ АУТОФАГИИ ЧЕРЕЗ РАЗЛИЧНЫЕ ПУТИ. КУРКУМИН ПОЛОЖИТЕЛЬНО ВЛИЯЕТ НА ЗАЩИТНУЮ АУТОФАГИЮ ЭПИТЕЛИАЛЬНЫХ КЛЕТОК КРОВЕНОСНЫХ СОСУДОВ ПРИ ОКИСЛИТЕЛЬНОМ СТРЕССЕ.
КУРКУМИН СПОСОБСТВУЕТ АУТОФАГИИ ЧЕРЕЗ РАЗЛИЧНЫЕ ПУТИ. КУРКУМИН ПОЛОЖИТЕЛЬНО ВЛИЯЕТ НА ЗАЩИТНУЮ АУТОФАГИЮ ЭПИТЕЛИАЛЬНЫХ КЛЕТОК КРОВЕНОСНЫХ СОСУДОВ ПРИ ОКИСЛИТЕЛЬНОМ СТРЕССЕ.Витамин D
Витамин D получают с помощью диеты, пищевых добавок и основная его часть синтезируются в коже при воздействии солнечных лучей. (46)
В экспериментах с мышами и на изолированных клетках витамин D индуцировал аутофагию в Β‑клетках поджелудочной железы, обеспечивая возможный путь для лечения сахарного диабета. Необходимы дополнительные исследования, чтобы определить, существует ли связь между витамином D, аутофагией поджелудочной железы и диабетом у людей. (47)
Омега-6 и омега-3 полиненасыщенные жиры
Добавки, содержащие омега-6 и омега-3 полиненасыщенные жиры, могут усиливать аутофагию. (48, 49)
В исследовании крыс с черепно-мозговой травмой омега-3 жирные кислоты способствовали аутофагии и предотвращали гибель нейронов в головном мозге. У червей омега-6 жирные кислоты увеличивают общую продолжительность жизни за счет активации аутофагии и замедления процессов старения. Излишне говорить, что эти результаты не были повторены у людей и должны быть приняты с долей скепсиса. (50, 51)
Никотинамид
Никотинамид является членом семейства витаминов группы В и ингредиентом для получения незаменимой энергетической молекулы Nicotinamide adenine dinucleotide (NAD, никотинамидадениндинуклеотида). В исследовании на мышах никотинамид задерживал прогрессирование снижения эффективности работы мозга и болезни Альцгеймера, увеличивая аутофагию в нейронах. (52)
В частности, его способность индуцировать аутофагическую рециркуляцию митохондрий может быть полезна для здоровья клеток. (53)
Литий
Литий – это химический элемент, который, имеет много преимуществ для здоровья при использовании его в качестве добавок к пище. Несколько исследований показали, что литий является частью аутофагии-стимулирующего сигнального пути у животных и людей (млекопитающих). Литий, по-видимому, индуцирует аутофагию путем ингибирования трифосфата инозитола (IP3), белка, играющего важную роль в пластичности нейронов мозга. (54, 55)
У животных литий усиливает деградацию агрегатно-склонных белков, которые вызывают болезнь Хантингтона, болезнь Альцгеймера и деменцию. Некоторые ученые связывают эти эффекты с увеличением аутофагии. (55)
Спермидин
Спермидин – это полиаминовое соединение, содержащееся в рибосомах и живых тканях. Спермидин в большом количестве также находится в разных продуктах питания. (56)
Уровень спермидина снижается с возрастом человека, создавая взаимосвязь между спермидином и многими маркерами старения. Кроме того, диеты с продуктами питания, насыщенные спермидином, связаны со снижением частоты сердечно-сосудистых заболеваний и рака. Было обнаружено, что спермидин активирует аутофагию у животных; поэтому некоторые ученые предположили, что он может индуцировать аутофагию и у людей, тем самым замедляя старение. (57)
Содержание спермидина в продуктах питания (мг/кг)
- Зародыш пшеницы – 243
- Соя (сушеная) – 207
- Сыр Чеддер (1 год выдержки) – 199
- Грибы – 89
- Рисовые отруби – 50
- Куриная печень – 48
- Зеленый горошек (свежий) – 48
- Манго – 30
- Нут – 29
- Цветная капуста (вареная) – 25
- Брокколи (вареная) – 25 (12)
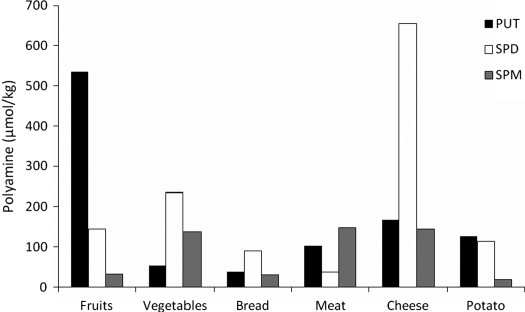 СОДЕРЖАНИЕ ПОЛИАМИНОВ В РАЗЛИЧНЫХ ПРОДУКТАХ ПИТАНИЯ. ПОЛИАМИНЫ: ПУТРЕСЦИН (черный), СПЕРМИДИН (белый), СПЕРМИН (серый) (источник)
СОДЕРЖАНИЕ ПОЛИАМИНОВ В РАЗЛИЧНЫХ ПРОДУКТАХ ПИТАНИЯ. ПОЛИАМИНЫ: ПУТРЕСЦИН (черный), СПЕРМИДИН (белый), СПЕРМИН (серый) (источник)Было обнаружен, что спермидин помогает с возрастным ухудшением здоровья и продлевает длительность жизни мух Drosophila melanogaster за счет активации аутофагии. (58)
Трегалоза (микоза)
Трегалоза (trehalose, микоза) – это углевод, дисахарид, который синтезируется некоторыми грибами, растениями, бактериями и беспозвоночными животными для получения энергии, а также, как средство выживания при сильных морозах и отсутствия воды.
Трегалоза индуцирует аутофагию и, как сообщается, ингибирует инфекцию цитомегаловирусом и обладает свойствами защиты нейронов. Большая часть исследований по трегалозе и аутофагии была сделана на клетках в пробирке, но одно исследование материнского диабета у животных показало, что трегалоза помогала поддерживать здоровый уровень аутофагии даже в присутствии избытка глюкозы в крови. (59, 60, 61)
Однако, нужно быть осторожным при приеме трегалозы. Как сообщалось в нескольких исследованиях трегалоза стимулирует рост Clostridium difficile (вид бактерий рода клостридий), которые являются главным возбудителем колита, инфекционного заболевания прямой кишки после приема антибиотиков. (17, 18)
Другие вещества
Многие соединения были связаны с повышением аутофагии в исследованиях на клетках. Однако, эти вещества не показали рост аутофагии при экспериментах на животных, не говоря уже о людях; поэтому доказательства их полезности имеют очень низкое качество и не должны использоваться в качестве основания для приема в любых медицинских целях. Мы включаем их сюда, потому что считаем интересным обратить внимание, какие вещества могут представлять интерес для будущих исследований.
Возможные вещества
- Кориноксин (Corynoxine), выделенный из Uncaria rhynchophylla, способствует клиренсу альфа-синуклеина через mTOR-путь. (62)
- Седрол (Cedrol), содержащийся в эфирном масле хвойных пород, индуцирует аутофагию и клеточную гибель клеток карциномы легких. (63)
- Экстракт амла из индийского крыжовника (Emblica officinalis) индуцирует аутофагию и ингибирует пролиферацию клеток рака яичников. (64)
- Экстракт гриба Санхван (Phellinus linteus) индуцирует аутофагию и ингибирует рост клеток рака молочной железы. (65)
- Экстракт европейского черного паслена (Solanum nigrum) индуцирует аутофагию и ингибирует клетки колоректальной карциномы. (66)
- Масло сандалового дерева индуцирует аутофагию и гибель клеток в пролиферирующих кератиноцитах кожи (предрак кожи). (67)
- Неферин (Neferine) из индийского лотоса (Nelumbo nucifera) индуцирует аутофагию через ингибирование сигнального пути PI3K /Akt /mTOR. (68)
- Анакардиевые кислоты, обнаруженные в оболочке ореха кешью (anacardium occidentale), индуцируют аутофагию и ингибируют клетки карциномы легких. (69)
- Нарингин, обнаруженный в цитрусовых фруктах (особенно в грейпфруте), индуцирует ингибирование через аутофагию роста раковых клеток. (70)
- Астин В (Astin B) из Астры татарской (Aster tataricus), индуцирует апоптоз и аутофагию в клетках печени. (7)
- Оридонин (Oridonin) из травы Rabdosia rubescens, индуцирует аутофагию и гибель клеток в клетках рака предстательной железы. (72)
Лекарственные препараты
Исследованиями было установлено, что некоторые лекарственные препараты индуцируют аутофагию в экспериментах на клетках или в опытах с животными; клинические испытания (и, следовательно, доказательства пользы для человека) – отсутствуют. Мы настоятельно обращаем внимание – не принимать ни один из этих препаратов без рецепта врача.
Лекарственные препараты, запускающие аутофагию
Некоторые лекарства нацелены на аутофагический путь. Они могут увеличить аутофагию, чтобы помочь очистить клетки от проблемных веществ (например, бактерий и дисфункциональных белков) или они могут использовать аутофагию в качестве средства индуцирования смерти раковых клеток.
Всегда консультируйтесь с врачом, прежде чем принимать какие-либо лекарства.
- Сиролимус, также известный как рапамицин, индуцирует аутофагию путем ингибирования mTOR. (73)
- Фентанил является мощным, синтетическим опиоидным обезболивающим препаратом, который индуцирует аутофагию через активацию пути ROS /MAPK. (74)
- Карбамазепин, лекарство, используемое в основном для лечения эпилепсии и невропатической боли, индуцирует аутофагию и, как было показано, действует на микобактерии туберкулеза с множественной лекарственной устойчивостью. (14)
- Метформин, препарат для лечения диабета, является аутофагическим промотором, который был опробован в лечении болезни Альцгеймера и, как сообщается, улучшает тревожное состояние. (75, 76)
- Иматиниб, химиопрепарат, используемый для лечения рака, индуцирует аутофагию в клетках хронического лейкоза. (77)
- Бортезомиб, противоопухолевый препарат, индуцирует аутофагию в клетках карциномы головы и шеи. (78)
Что подавляет механизм аутофагии
Были обнаружены некоторые вещества, которые уменьшают аутофагию в опытах на животных или в клеточных исследованиях, но это не говорит о том, что следует их избегать людям. Этот раздел статьи не должен использоваться в качестве основания для того, чтобы принимать или избегать конкретное вещество или лекарство. Поговорите с вашим доктором перед приемом любого нового вещества, и ни при каких обстоятельствах не прерывайте лечение с помощью лекарства, не посоветовавшись с врачом.
Биологические вещества
Отказ от ответственности редакции КОД ЖИЗНИ
- Эвгенол, фенольная кислота, найденная в гвоздике (Syzygium aromaticum), была была выявлена среди 86 традиционных китайских лекарств, как имеющая самую сильную способность уменьшать аутофагию. (79)
- Сообщается, что Бафиломицин A1, макролидный антибиотик, полученный из Streptomyces griseus, ингибирует аутофагию. (80)
- Elaiophylin был определен, как соединение микробного происхождения корпорации North China Pharmaceutical Group Corporation, которые имеет хорошую способность уменьшать аутофагию. (8)
- Oblongifolin C, феноловая кислота из азиатского дерева Garcinia yunnanensis, ингибирует аутофагию и описан как обладающий противоопухолевыми свойствами. (82)
- Matrine, алкалоид, обнаруженный в растениях из рода Sophora, является ингибитором аутофагии (через модуляцию лизосомального процесса). (83)
Лекарственные препараты
- Вортманн (84)
- 3-метиладенин (85)
- Спаутин-1 (86)
- Кломипрамин (87)
- Lucanthone (88)
- Хлорохин (89)
Информация на этом сайте не была оценена какой либо медицинской организацией. Мы не стремимся диагностировать и лечить любые болезни. Информация на сайте предоставляется только в образовательных целях. Вы должны проконсультироваться с врачом, прежде чем действовать исходя из полученной информации из этого сайта, особенно, если вы беременны, кормящая мать, принимаете лекарства, или имеете любое заболевание.
Оцените эту статью
Среднее 4.8 Всего голосов (8)Как ускорить метаболическую аутофагию и почему
Аутофагия – это биологический процесс, при котором части клеток перерабатываются и превращаются в запасные клетки. Это механизм утилизации, который предотвращает накопление старых и изношенных органелл. Аутофагия активируется во время голодания и недостатка энергии. Всякий раз, когда вашему организму не хватает жизненно важных питательных веществ, активируется аутофагия, позволяющая ему перерабатывать компоненты. Вы можете получить аналогичные результаты с помощью периодического и обычного голодания.
Сийм Лэнд, социокультурный антрополог, предприниматель и тренер высокой эффективности, который также является автором превосходной книги «Метаболическая аутофагия: практикуйте периодическое голодание и тренировки сопротивления для наращивания мышечной массы и повышения продолжительности жизни (Книга о диете спомощью метаболической аутофагии)».
Джозеф Меркола: Аутофагия и метаболизм
Я встретился с Лэндом на мероприятии Дейва Аспри в 2019 году в Upgrade Labs, формально известном как Пуленепробиваемая конференция, и был впечатлен глубиной его познаний. «Метаболическая аутофагия» — замечательное дополнение к книге «Жир в качестве топлива: революционная диета для борьбы с раком, ускорения работы мозга и повышения энергии».
Подписывайтесь на наш аккаунт в INSTAGRAM!
Тем не менее, она хороша и сама по себе, так как она в деталях описывает конкретные протоколы, которым вы должны следовать. Важно отметить, что она проясняет одно из основных заблуждений относительно аутофагии о том, что, поскольку она полезна, вы должны активировать ее постоянно. Это не соответствует действительности и может иметь неприятные последствия, особенно если вы – человек в возрасте.
Один из способов оставаться в аутофагии — свести к минимуму количество белка, и если вы находитесь на постоянной диете с низким содержанием белка, вы никогда не активируете анаболизм, т.е. строительство мышечной ткани. Лэнд великолепно расправляется с этой путаницей и предоставляет конкретные протоколы цикличности, которые помогут вам поддерживать вашу мышечную массу и получить все преимущества аутофагии.
Аутофагия для чайников
Вкратце, аутофагия переводится как «самопоедание». Это биологический процесс, в котором части ваших клеток перерабатываются.
«Проще говоря, это механизм переработки, который предотвращает накопление старых и изношенных органелл, будь то расщепленные митохондрии, активные формы кислорода [или] воспалительные цитокины», — объясняет Лэнд.
«Аутофагия — это процесс, через который проходит ваше тело, когда оно хочет, или когда ему нужно восстановить и излечить себя. Он играет важную роль во многих заболеваниях, от которых мы страдаем. Аутофагия может принести пользу при таких состояниях, как резистентность к инсулину [и] заболевания печени.
Даже болезнь Альцгеймера и сердечная недостаточность в некоторой степени связаны с процессами аутофагии. Ее дефицит, как было показано, является причинным и способствует развитию этих заболеваний».
Как активировать аутофагию
Аутофагия активируется во время голодания и недостатка энергии. Всякий раз, когда ваше тело испытывает недостаток важных питательных веществ, таких как аминокислоты, белки, карбид, глюкоза или углерод, а это неполный список, активируется аутофагия, позволяющая вашему организму перерабатывать эти компоненты.
Также в игру вступают другие нижестоящие пути, такие как сиртуины, АМФ-активируемая протеинкиназа (АМФК) и FOX-белки, чтобы поддержать этот омолаживающий процесс. «Все они оказались центральными компонентами долголетия, когда речь идет о таких вещах, как ограничение калорий и физические упражнения», — говорит Лэнд.
Хорошей новостью является то, что ограничение калорий не является необходимым. Вы можете получить те же результаты с помощью периодического и обычного голодания. Ограничение калорий также имеет недостатки, такие как, например, дефицит питательных веществ, слабость, потеря мышечной массы и плотности костей, которые обходятся стороной при периодическом голодании.
Как и я, Лэнд использует ограниченное время приема пищи, съедая все в течение четырех часов каждый день. Я использую окно от четырех до пяти часов. Важно отметить, что это не то же самое, что ограничение калорий. Вы не ограничиваете количество потребляемых калорий; вы просто ограничиваете время, в которое вы их едите, и, таким образом, вы можете активировать аутофагию.
Аутофагия легко нарушается едой
Важно поддерживать близкое к нулю количество калорий, которое не повысит ваш инсулин и не переведет вас в анаболическое состояние (то есть в состоянии сытости). Другими словами, голодание позволяет вашему телу оставаться в аутофагии. Конечно, есть степени ингибирования в зависимости от типа питательных веществ, которые вы едите. Лэнд объясняет:
«Статус питательных веществ постоянно контролируется цензорами топлива, такими как mTOR, основной путь роста. Противоположностью этому является АМФК. Они, как инь и ян вашего метаболизма, постоянно следят за тем, какое топливо сгорает в крови.
Основываясь на этой информации, они решают, будут ли они расти или активировать аутофагию, чтобы перерабатывать себя. В течение дня эти топливные датчики уравновешивают друг друга, поэтому они не могут сосуществовать.
Всякий раз, когда вы съедаете бейгл, он повышает уровень инсулина и активирует путь mTOR, что переводит вас в состояние насыщения и препятствует аутофагии.
Но в то же время, если вы едите что-то более кетогенное, это приведет к значительно более низкому анаболическому ответу, потому что инсулин не повышается и в организм не поступают лишние аминокислоты.
Таким образом, есть определенная степень [ингибирования аутофагии], при том, что большое количество углеводов и белка являются более анаболическими и сильнее стимулирующими mTOR. Пища с низким содержанием углеводов, умеренным – белков и высоким – жира, будет сильнее стимулировать АМФК, [таким образом] она может поддерживать аутофагию дольше или намного легче».
Подписывайтесь на Эконет в Pinterest!
Конечно, от продолжительности голодания также будет многое зависеть. Например, после 24- или 48-часового поста ваш АМФК будет намного выше, а mTOR значительно сильнее подавлен, чем после 16-часового голодания. В этом случае ваша буферная зона будет больше, а это означает, что определенные продукты не окажут столь сильного влияния на аутофагию.
Персональная программа Лэнда
Лэнд, который имеет телосложение опытного гимнаста, является отличным примером для подражания, и показывает, как хорошо спланированная программа, которая циклично проходит через аутофагию и анаболизм, может преобразить ваше тело. Его собственная программа, как правило, состоит из 20 часов голодания в день и еды в течение четырех часов.
Когда он перестает голодать раньше, скажем, через 16 или 18 часов вместо 20, он делает это, выпивая костный бульон или что-то подобное. Это нарушает пост, но не полностью. «Я по-прежнему буду поддерживать состояние полу-голодания до тех пор, пока у меня не останется калорий», — говорит он. Он также рассеивает опасения по поводу потери мышечной массы в результате голодания.
Катаболизм / анаболизм — вам нужны оба, но не одновременно
Вы можете активировать два различных метаболических пути: аутофагия (катаболизм, разрушение или восстановление ваших тканей) и mTOR (анаболизм, который является процессом восстановления). Путь mTOR по существу является чувствующим белки путем, который активируется белком и инсулином.
Раньше я был чрезмерно обеспокоен активацией mTOR, думая, что, вероятно, лучше ее избегать по максимуму, так как он является основной движущей силой хронических заболеваний и старения. Это не совсем верно, и книга Лэнда отлично рассеивает это распространенное заблуждение.
Как и в случае с аутофагией, нужно, чтобы mTOR был активирован не постоянно, но периодически.
Если вы проходите двухдневное голодание, это не время для тяжелых тренировок с нагрузкой, потому что это приведет к попытке активировать анаболизм и аутофагию одновременно. Это похоже на одновременное нажатие на педаль тормоза и газа, а это не очень хорошая идея. Итак, во время голодания помните, почему вы это делаете. Лэнд объясняет:
«Вы не можете нарастить мышечную массу с помощью длительного голодания. Его цель — углубиться в аутофагию и, по сути, способствовать клеточному очищению [и] исцелить себя.
В этот момент я не вижу смысла в попытках проводить напряженную тренировку с отягощениями, потому что, во-первых, у вас недостаточно энергии, чтобы достичь личного рекорда. Во-вторых, ваше тело не будет реагировать на это так же положительно. Скорее всего вы просто добавите дополнительную нагрузку на тело.
Во время продолжительного голодания я люблю проводить несколько более легких тренировок с массой тела или фитнес-резинками, просто чтобы стимулировать мышцы. Это сигнализирует организму о том, что ему по-прежнему необходимо сохранять больше мышечной ткани.
Если я буду выполнять утомительную тренировку, а потом ничего не буду есть, я настрою себя на провал. Это неизбежно приведет к усилению катаболизма мышц».
Выбор времени и польза анаболизма
Когда дело доходит до наращивания мышечной массы, время активации анаболизма может иметь большое значение. Чтобы его оптимизировать, нужно выполнять тяжелую тренировку с отягощениями, находясь в голодном состоянии, а затем заново наполнить организм пищей сразу после этого.
Как отмечает Лэнд, тренировка на голодный желудок может немного снизить вашу максимальную производительность, но вам не нужно тренироваться на максимуме, чтобы улучшить силу и мышечное развитие.
Тем не менее, есть некоторая польза от потребления небольшого количества белка прямо перед тренировкой. После этого обсуждения в книге Лэнда я начал есть два сырых яйца до начала упражнений.
«Для роста и сохранения мышц определенно стоит иметь некоторые аминокислоты и белок в системе, пока вы тренируетесь. Много не нужно. Вероятно, хватит и 10 грамм. Этого будет достаточно, и это не вызовет резкий всплеск инсулина. Это не выбьет вас из голодного состояния полностью», — говорит Лэнд.
Основы гормезиса
Лэнд также отлично справляется с определением гормезиса в своей книге. Это важная концепция, которую можно сформулировать так: «Все, что не убивает вас, делает вас сильнее». Это биологическая стратегия, которая позволяет вашему организму адаптироваться к стрессовым воздействиям окружающей среды, например, к ограничению калорий, к голоданию, холоду или жаре.
Гормезис также производит эффекты, подобные аутофагии, потому что он стимулируется аналогичными путями, включая АМФК, FOX-белки и сиртуины. Например, прерывистое голодание – это мягкий стрессор, который активирует гормезис. Высокоинтенсивное упражнение — другой, более интенсивный активатор.
В нашем интервью мы также обсудим другие преимущества саун ближнего инфракрасного диапазона и белков теплового шока, которые являются следствием аутофагии. Таким образом, основная функция белков теплового шока заключается в правильном фолдинге белков, что является одной из причин, почему сауна-терапия так полезна для общего состояния здоровья. Тепло также стимулирует аутофагию.
Подберите стратегию для своего возраста
Мы также обсуждаем важность никотинамидадениндинуклеотида (NAD+), кофермента, обнаруженного во всех клетках, который необходим для биологических процессов, включая энергетический гомеостаз. В молодости прием добавки NAD не обязателен, но с возрастом его уровень начинает снижаться.
Одним из крупнейших потребителей молекулы NAD+ является поли(АДФ-рибоза)-полимеразы (PARP), фермент восстановления ДНК. В настоящее время я исследую эту проблему, и кажется, что доза при терапии повышения уровня NAD сильно зависит от вашего возраста.
Людям до 30 или 40 лет, скорее всего, она не понадобится, если нет хронической проблемы со здоровьем. Однако, когда вам за 40, повышение уровня NAD становится важной стратегией.
Хорошей новостью является то, что есть много способов естественного повышения уровня NAD, таких как физические упражнения, которые резко увеличивают ограничивающий скорость образования фермент NAD, называемый никотинамидфосфорибозилтрансферазой или NAMPT. Голодание также увеличит уровень NAD, что является еще одним из его преимуществ.
Подписывайтесь на наш канал VIBER!
Проблема, с которой сталкивается большинство людей, заключается в том, что они прекращают или радикально сокращают физические нагрузки, когда становятся старше. Хрупкость, которая ассоциируется со старостью, отчасти связана с накоплением никотинамида, который не превращается обратно в NAD. Он также ингибирует важные для долголетия белки сиртуины. Как только вы перестаете получать преимущества сиртуинов и NAD, продолжительность жизни сокращается.
Потребность в белке увеличивается с возрастом
Это важный момент, о котором Лэнд подробно рассказывает в своей книге. Уровень белка, в частности, меняется с возрастом, и для поддержания мышечной массы потребуются разные стратегии в зависимости от вашего возраста. По мере старения, наряду со снижением уровня НАД, вы также заметите снижение уровня гормона роста, а также способности синтезировать белок и строить ткани.
Лэнд также рекомендует циклически менять количество белка, которое вы потребляете. Например, в день голодания количество белка может быть небольшим, потому что он не нужен для восстановления мышц, тогда как более высокое потребление белка принесет вам наибольшую пользу в дни, когда вы выполняете силовые тренировки.
Лэнд рекомендует потребление минимум 0,6 г и максимум 0,8-1,0 г белка на фунт мышечной массы.
Чтобы рассчитать мышечную массу тела, определите процент жира в организме и вычтите его из общего веса. Итак, если у вас 20% жира, то ваша мышечная масса будет составлять 80% от общего веса. Затем умножьте это на, скажем, 0,8 грамма, чтобы рассчитать потребность в белке.опубликовано econet.ru.
Автор Джозеф Меркола
Подписывайтесь на наш youtube канал!
P.S. И помните, всего лишь изменяя свое сознание — мы вместе изменяем мир! © econet
история исследований и Нобелевская премия 2016 – ответы на главные вопросы
Между гомологичными генами дрожжей и млекопитающих есть существенное сходство. Белковые продукты этих генов отличаются небольшим количеством аминокислотных замен. Если какой-то ген у дрожжей отвечает за аутофагию, то, скорее всего, похожий ген у животных и человека будет выполнять подобные функции. Генетику аутофагии было проще исследовать в дрожжевых клетках. Но параллельно с изучением механизмов аутофагии у дрожжей в лаборатории, возглавляемой Ёсинори Осуми, были обнаружены гомологи ряда дрожжевых генов ATG в клетках млекопитающих. Исследование функционирования белков млекопитающих, кодируемых этими генами, показало, что молекулярные механизмы аутофагии высококонсервативны у эукариот, то есть мало отличаются у таких эволюционно далеких организмов, как дрожжи и человек.
В лаборатории Ёсинори Осуми при изучении белка LC3 млекопитающих, гомолога дрожжевого белка ATG8, были обнаружены процессированная (укороченная) и липидированная формы белка — LC3-I и LC3-II соответственно. Эти формы в настоящее время стали популярными маркерами аутофагосом и индикаторами аутофагии. Далее была создана трансгенная мышь, экспрессирующая рекомбинантный белок, состоящий из LC3 и зеленого флуоресцирующего белка GFP. Это позволило легко визуализовать аутофагию с помощью флуоресцентной микроскопии и изучить кинетику и интенсивность аутофагии в разных органах мыши при голодании. В лаборатории Ёсинори Осуми была также впервые создана мышь с нокаутированным ATG геном. Гомозиготные мышата с нокаутированным ATG5 рождались нормально, но погибали в течение 24 часов после рождения. Это показало, что аутофагия существенна для неонатального развития у млекопитающих. Созданные в лаборатории Ёсинори Осуми трансгенные по GFP-LC3 и одновременно нокаутированные по ATG5 мыши успешно используются мировым научным сообществом для изучения физиологического значения аутофагии у млекопитающих. Ёсинори Осуми также принял участие в идентификации гомологов генов ATG у высших растений и в демонстрации их участия в аутофагии, что еще раз подтвердило консервативную и фундаментальную роль аутофагии у эукариот.
Типы и механизмы аутофагии
Существует три типа аутофагии: макроаутофагия, микроаутофагия и шаперон-зависимая аутофагия. При микроаутофагии мембрана лизосомы образует впадину, в которую попадает часть цитоплазмы, а затем эта впадина замыкается, образовавшийся пузырек транспортируется внутрь лизосомы, где происходит деградация его содержимого. При шаперон-зависимой аутофагии комплексы дефектных белков с шаперонами попадают в лизосомы при участии специфических мембранных рецепторов.
Ёсинори Осуми получил Нобелевскую премию за исследования макроаутофагии, которую обычно называют просто аутофагией. Под действием сигналов, инициирующих макроаутофагию, образуется так называемый фагофор, который состоит из липидной мембраны и ряда белков, кодируемых генами ATG или гомологами генов ATG. С помощью сложной системы регуляции к фагофору привлекаются новые ATG-белки, собираются мультикомпонентные комплексы, мембрана растет, и образуется незамкнутая структура, по форме напоминающая шапочку, которая окружает часть цитоплазмы (см. рисунок). Затем двухслойная мембрана замыкается, и внутри получившегося пузырька, называемого аутофагосомой, оказываются макромолекулы и органеллы (рибосомы, митохондрии, фрагменты эндоплазматического ретикулума). Образовавшаяся аутофагосома сливается с лизосомой и образует аутофаголизосому, внутри которой происходит деградация макромолекул и органелл. В этом процессе участвуют белковые продукты более 30 генов ATG, существенная часть которых была открыта в работах Ёсинори Осуми.
Аутофагия | Блог 4brain
Очищение организма от вредных веществ – вопрос, которому сегодня уделяют много внимания, причем не только ученые, но и обычные обыватели. И чего только не делают люди, казалось бы, во благо самим себе: пьют очищенные соки, сидят на детокс-диетах, пьют огромное количество воды, делают клизмы, употребляют всевозможные лекарственные препараты и колдуют над плитой, поглядывая на бумажки с народными рецептами.
Но все ли это эффективно? Безусловно, правильное питание, питьевой режим, гречка и овсянка полезны, однако не стоит ожидать, что они выведут из организма токсины и шлаки намного быстрее, чем обычное питание. Что же делать? А делать вот что – можно обратиться к пока еще не очень известному, но очень эффективному способу очищения своего организма, который, ко всему прочему, можно еще и контролировать самостоятельно.
Заключается этот способ в… самопоедании! Да, да, вы все правильно прочитали – в самопоедании (или самоканнибализме). Но лучше все же называть это научным термином «аутофагия». При желании вы можете научить свое тело самостоятельно избавляться от вредных веществ. Но не будем торопиться, и расскажем обо всем по порядку.
Что за самопоедание такое?
Понятие «аутофагия», если перевести его с греческого языка, означает «самопоедание». Суть этого процесса кроется в утилизации (переработке) макромолекул и органелл (компонентов, необходимых для существования клеток) в клеточных компартментах (обособленных областях), которые образуются при слиянии лизосом (клеточных органоидов) с аутофагосомами (структурами, образующимися вокруг поврежденных клеток). Но это сугубо научное определение.
Если говорить проще, то при аутофагии происходит адаптация клеток к тяжелым условиям. Если питательных веществ, поступающих извне, в организме недостаточно, клетка отдает немного своих органелл и макромолекул для получения мономеров – элементов, подходящих для синтеза новых белков, нуклеиновых кислот, углеводов и липидов.
Процесс аутофагии очень важен для удаления из клеток поврежденных элементов, таких, например, как белковые агрегаты. По мере протекания этого процесса, поврежденные органеллы и макромолекулы, находящиеся в цитоплазме, попадают в особый компартмент, где происходит их расщепление на малые молекулы. И уже эти малые молекулы, если имеет место недостаток энергии и голодание, становятся строительным материалом, из которого образуются новые органеллы и биополимеры (белки, нуклеиновые кислоты, полисахариды и другие элементы, необходимые для работы организма).
Аутофагией сопровождается жизнедеятельность всех нормальных клеток в обычных условиях. Однако чрезмерная аутофагия способна привести к смерти клетки, по причине чего сегодня она рассматривается в качестве одной из форм программируемой клеточной гибели вместе с такими процессами как некропотоз и апоптоз.
И, наконец, если говорить совсем просто, можно сказать так: с течением времени в каждой клетке нашего организма скапливается «мусор», а аутофагия способствует его переработке и, как следствие, омоложению организма. Все элементарно. «Но как же так? Почему никто об этом не говорит? Почему не трубят во всеуслышание СМИ?» – вполне резонные вопросы. Но об этом и говорят, и СМИ тоже прекрасно об этом знают. Просто ошеломляющие результаты, к которым приводит аутофагия, стали известны совсем недавно.
Открытие аутофагии: исследования Кристиана де Дюва
Вообще об аутофагии, как о способе доставки цитоплазматического материала клетки в лизосомы для последующей деградации, известно с 1963 года. Тогда этот термин ввел первооткрыватель лизосом – бельгийский биохимик Кристиан де Дюв. И здесь нам нужно снова вернуться к научной терминологии – для истории открытия это очень важно.
В результате исследований де Дюв обнаружил, что при аутофагии в цитоплазме сначала происходит процесс формирования аутофагосом – пузырьков, которые окружает двухслойная мембрана, и которые содержат в себе часть цитоплазмы и клеточные органеллы, такие как фрагменты эндоплазматического ретикулума, рибосомы и митохондрии. После этого аутофагосомы объединяются с лизосомами, образуя аутолизосомы. В них под действием лизосомных ферментов (гидролаз) деградируют органеллы и макромолекулы.
За эти открытия в области структурной и функциональной организации клетки в 1974 году де Дюв получил Нобелевскую премию.
Дальнейшие исследования аутофагии: работа Есинори Осуми

И вот в не таком еще далеком 2016 году выдающийся японский ученый – молекулярный биолог Есинори Осуми – стал изучать аутофагию в дрожжевых клетках, применяя для этого генетический подход. В результате он нашел более десятка генов, инактивация (полная или частичная потеря веществом своей активности) которых вызывала дефекты аутофагосом. Найденные гены были изучены и клонированы.
Дальнейшие изыскания в области функционирования белковых продуктов данных генов позволили выяснить молекулярные механизмы появления, протекания и регуляции аутофагии. Кстати, найденные Осуми гены получили название ATG (от англ. «autophagy-related genes»), и к настоящему времени их найдено свыше тридцати.
Есинори Осуми продемонстрировал, что аутофагия является запрограммированным процессом, т.е. таким процессом, который кодируется в геноме. Если же отключить или мутировать гены, необходимые для аутофагии, протекание этого процесса станет невозможным. Но какое отношение все это имеет к здоровью человека с точки зрения обывателя?
Дело в том, что гомологичные гены дрожжей и млекопитающих обладают ощутимым сходством. Белковые продукты таких генов отличает небольшое количество аминокислотных замен. Если определенный ген у дрожжей ответственен за аутофагию, то велика вероятность, что подобный ген будет выполнять аналогичные функции и у человека.
Генетика аутофагии должна была исследоваться в дрожжевых клетках – это намного проще. Однако вместе с исследованием механизмов аутофагии у дрожжей в своей лаборатории Осуми обнаружил гомологи некоторых дрожжевых генов ATG в клетках млекопитающих. Изучение функционирования их белков, которые кодируются этими генами, показало ученым, что различия в молекулярных механизмах аутофагии у таких совершенно разных организмов, как дрожжи и человек, ничтожно малы.
После определенных научных манипуляций и последующего обнаружения новых форм белка, команда Осуми создала трансгенную мышь, преобразующую наследственную информацию от гена в рекомбинантный белок. Это позволило визуализировать аутофагию при помощи флуоресцентной микроскопии и изучить ее кинетику и интенсивность в разных органах мыши во время голодания. И уже следующие исследования, для которых создавались мыши с отключенным геном ATG, помогли узнать, что аутофагия имеет огромное физиологическое значение для развития млекопитающих, в том числе и человека.
В 2016 году Есинори Осуми был награжден Нобелевской премией «За открытие механизмов аутофагии». Вот небольшое видео об этом:
А в 2017 году его наградили Премией за прорыв в области медицины. И это не случайно, ведь его работа способна вывести всю мировую медицину на принципиально новый уровень. Но прежде чем мы приступим к рассмотрению пользы аутофагии для здоровья человека, нужно сказать несколько слов и о ее типах.
Типы аутофагии
Современные ученые выделяют три типа аутофагии – это микро- и макроаутофагия, а также шапероновая аутофагия:
- Микроаутофагия. Обломки клеточных мембран и макромолекулы захватываются лизосомой. Благодаря этому при нехватке строительного материала и энергии (например, когда человек голодает) клетка способна переваривать белки. Однако механизмы микроаутофагии активизируются и в нормальных условиях.
- Макроаутофагия. Часть цитоплазмы (чаще всего та, которая содержит органоиды) окружается мембранным компартментом. В итоге эта часть двумя мембранами отделяется от остальной цитоплазмы, превращаясь в аутофагосомы. Они объединяются с лизосомами и образуют аутофаголизосомы, где перевариваются органеллы и прочее содержимое аутофагосом. При помощи этого вида аутофагии клетки могут избавляться от органоидов, которые «отслужили свой срок».
- Шапероновая аутофагия. Частично денатурировавшие белки целенаправленно транспортируются из цитоплазмы в полость лизосомы для последующего переваривания. Инициировать данный тип аутофагии (кстати, описан он лишь для млекопитающих) можно с помощью стресса, например, серьезными физическими нагрузками или голоданием.
И теперь мы наконец-таки можем немного отойти от специфической научной терминологии, и поговорить на «человеческом» языке конкретно о влиянии аутофагии на организм человека.
Польза аутофагии для человека
Положительная роль аутофагии для человеческого здоровья, конечно же, преобладает над отрицательной, иначе бы ей не уделялось столько внимания. Но чтобы адекватно представить себе ее благотворное воздействие, нужно вспомнить кое-что о природе ее появления.
До того как появились технологии выращивания продуктов почти в любых условиях и их длительного хранения, завися от климата, в определенные периоды (ранняя весна и зима) люди должны были ограничиваться в питании. Вместе с тем они прекрасно себя чувствовали, а о повальном распространении таких серьезных заболеваний как болезнь Альцгеймера, рак или туберкулез говорить не приходилось. А как мы с вами уже успели выяснить (пусть сказали об этом пока лишь вскользь), клетки начинают переваривать «отработанный» материал, шлаки и токсины именно при голодании.
Согласно все тем же научным исследованиям (а также процессу эволюции), положительная роль аутофагии неоспорима, т.к. низкокалорийная диета примерно на 30-40% увеличивает продолжительность человеческой жизни. Ограничения в питании, с научной позиции, активизируют выработку организмом особых генов, отвечающих за долголетие и способствующих продолжению жизни даже в условиях относительно скудного питания.
Есть все основания полагать, что аутофагия представляет собой внутреннюю программу переработки вредных веществ в организме. Она повышает эффективность организма, избавляя его от нефункционирующих частиц, останавливая развитие раковых клеток и препятствуя метаболическим дисфункциям, например, диабету или ожирению.
Есть также данные о том, что аутофагия имеет серьезное значение для контроля иммунной системы и воспалительных процессов. Вспомните тех самых мышей с неработающим геном ATG – у них наблюдалась сонливость и ожирение, мозговые нарушения и повышенный уровень холестерина. А все мы знаем, что такие «особенности» способны привести к самым серьезным и отнюдь не радостным последствиям. И, раз уж мы упомянули рак, то и о его связи с аутофагией следует поговорить.
Аутофагия и рак
Ученые из университета Пенсильвании, занимающиеся поиском эффективного средства против рака, сделали еще один важный шаг благодаря данным об аутофагии. Теперь они могут с полным правом говорить о том, что создание на самом деле работающего метода борьбы с онкологическими заболеваниями не за горами.
В частности, исследователи работали с лизосомным ферментом PPT1, и с его помощью им удалось разработать лекарственный препарат, показавший высокие результаты в борьбе с такими заболеваниями как колоректальный рак, опухоль поджелудочной железы и меланома. Но пока все опыты, опять же, были проведены на мышах.
Этот самый фермент PPT1 отвечает за два важнейших процесса в жизнедеятельности и росте раковых клеток. Первый процесс – это сама аутофагия, позволяющая выживать онкоклеткам, а второй – мишень рапамицина (mTOR), отвечающая за неконтролируемый рост опухолей. Кстати, препараты, которые применяются в последние годы, тоже направлены на мишень рапамицина, но отличие их в том, что процесс аутофагии они не учитывают, из-за чего нет возможности повлиять на устойчивость онкоклеток к лечению.
Теперь же, благодаря открытиям Есинори Осуми, показавшим, что можно «заставить» клетки поедать самих себя, избавляться от поврежденных частиц и получать новые ресурсы для восстановления, ситуация в корне изменилась. Ученые обнаружили, что mTOR тоже может использовать аутофагию, чтобы обеспечить себе ресурсы, а при воздействии на фермент PPT1 активность первого подавляется, и процесс аутофагии блокируется. Это и есть причина, по которой раковая опухоль начинает воспринимать противораковую терапию.
Однако все эти достоинства аутофагии – лишь одна сторона медали. Очень важно понимать и всегда помнить о том, что она может сказаться на состоянии организма и отрицательно. Правда, касается это лишь определенной категории людей.
Вред аутофагии для человека
Перед тем как принять решение запускать и стимулировать процесс аутофагии в своем организме, в обязательном порядке убедитесь в том, что у вас нет:
- Хронических заболеваний (в частности, заболеваний ЖКТ)
- Гастрита
- Язвы
- Отклонений в массе тела (случаи, когда она ниже нормы)
- Дефицита иммунитета
- Диабета
- Ишемической болезни сердца
- Депрессии
- Гипотонии (пониженного давления)
- Психических нарушений
Кроме того, активизировать аутофагию категорически запрещается женщинам, у которых имеются проблемы с фертильностью и лактацией, беременным женщинам и людям, принимающим лекарства, не совместимые с голоданием. Если пренебречь этими противопоказаниями, можно серьезно ухудшить состояние своего организма, усугубить уже имеющиеся недуги и серьезно подорвать здоровье. В остальном же, как утверждают ученые, аутофагия – это вполне безопасный способ очищения и омоложения. Не менее радует и то, что запустить ее можно самостоятельно.
Как запустить аутофагию: аутофагия и голодание

Большинство современных людей, злоупотребляя высококалорийной, нездоровой и неполезной пищей, сами делают так, что процесс аутофагии просто не запускается. А это, если серьезно задуматься, как раз-таки и ведет к снижению иммунитета, ускорению старения и даже развитию всевозможных мутаций на клеточном уровне.
Если же заставить клетки голодать, они автоматически начнут использовать внешние ресурсы для функционирования, избавляться от вредных веществ и восстанавливаться. Но и постоянное недоедание может привести к дегенеративным процессам, ведь аутофагия просто не остановится. Поэтому есть смысл частично возвратиться к идеям лечебного голодания.
Всего можно выделить несколько его видов, но нас интересуют именно два – это прерывистое и пролонгированное голодание. Именно их подробно описал известный итальянско-американский биогеронтолог и клеточный биолог Вальтер Лонго, много лет занимавшийся исследованиями воздействия голодания и ограниченной диеты на продолжительность жизни и здоровье (имейте в виду, что говоря о голодании, мы имеем в виду отказ конкретно от пищи, но не от воды).
Прерывистое голодание
Суть прерывистого голодания: сутки без пищи, за которыми следует 1-2 суток нормального питания.
Научные исследования говорят о том, что благодаря прерывистому голоданию активизируются нервные связи и улучшаются когнитивные функции, снижается артериальное давление и частота сердечных сокращений, повышается чувствительность тканей к инсулину, задерживается появление опухолей, предотвращаются воспалительные заболевания, улучшается регенерация крови, увеличивается число белых клеток в крови и стимулируется иммунная система.
Опыты, проведенные с уже не раз упомянутыми мышами, подтвердили пользу прерывистого голодания как профилактики нейродегенеративных, сердечно-сосудистых и опухолевых заболеваний, а также сахарного диабета. А последующее наблюдение уже за людьми показало, что оно нормализует артериальное давление и уровень глюкозы, снижает количество маркеров воспаления у страдающих бронхиальной астмой.
Не стоит, конечно, отказываться от популярной сегодня диетологической нормы питания часто и понемногу, но все же нужно иметь в виду, что из-за такого режима усиливается выработка инсулина, отчего клетки теряют к нему чувствительность, а это может привести к сахарному диабету второго типа. Так что даже эту норму (питаться часто и понемногу) полезно время от времени разбавлять периодическим голоданием.
Пролонгированное голодание
Суть пролонгированного голодания: 2-3 (иногда больше) суток без пищи, за которыми следует как минимум 7 дней перерыва до следующих 2-3 суток голодания.
Здесь снова вступают в силу результаты научных исследований. Они говорят о том, что пролонгированное голодание приводит к активизации аутофагии, повышению чувствительности опухолей к терапии, улучшению регулирования уровней инсулина (и инсулиноподобного фактора роста 1) и глюкозы.
Также голодание по такой схеме снижает массу печени и количество лейкоцитов в крови. Но возобновление питания продуцирует мощные процессы регенерации, как в иммунной системе, так и в печени. По этой причине пролонгированное голодание допускается лишь под контролем специалиста. Особую же осторожность в этом случае необходимо соблюдать людям старше 65 лет, т.к. в этом возрасте недостаток белков может вызвать нежелательную потерю мышечной массы.
Вот еще несколько рекомендаций касаемо безопасного ограничения диеты:
- Даже при полном отказе от питания на сутки и более необходимо пить достаточное количество воды
- Очень удобный и безопасный способ стимулирования аутофагии заключается в отказе от 1-2 приемов пищи (например, ужина и/или обеда) 2-3 раза в неделю
- При имитации периодического голодания в течение 5 дней (еще один совет от Вальтера Лонго) необходимо употребить не более 100 калорий в первый день и по 500 калорий – в оставшиеся четыре дня
И, конечно же, говоря о диете, мы не могли упустить вопрос на тему правильности и неправильности питания вообще. Все мы уже по сотне раз слышали, что нельзя есть после 18 часов. И с позиции новых данных, полученных об аутофагии Есинори Осуми, это утверждение снова подтверждается, а вот вопрос о пользе частого дробного питания остается открытым.
Вернемся к нашим мышам, которые оказывают существенную помощь в исследованиях по улучшению здоровья человека. Опыты показали, что при одинаковом количестве калорий в сутки мыши, которые питались с интервалом в 12 часов, «показывали» лучшие результаты, нежели те, которые питались часто и понемногу. Так, у мышей первой группы наблюдалось улучшение циркадных ритмов и они лучше спали, но главное – у них переставали развиваться и даже обращались вспять метаболические заболевания.
Это в очередной раз говорит о том, что если вдруг в течение дня вы не успеваете поесть, имея возможность питаться лишь утром и/или вечером, нужно не расстраиваться, а радоваться, ведь так вы запускаете аутофагию на благо своему организму. Точно так же и питание с перерывами в 12 и более часов активизирует аутофагию. Как бы странно это не звучало, но такой режим питания способствует снижению жировой массы без потери мышечной, снижению в крови уровня глюкозы и холестерина. А голодание свыше 13 часов в период с вечера до утра минимизирует риск развития рака груди.
Но здесь мы хотим заметить: ни в коем случае не следует воспринимать аутофагию в качестве лекарства. По большей части это профилактика разных недугов, но никак не их лечение. Имейте это в виду и не делайте ложных выводов.
Кстати, можете посмотреть видео «Голодание с разных ракурсов/Голодание как основа жизни», из которого можно узнать немало любопытных фактов о голодании и его воздействии на организм:
Если же вам совсем не хочется голодать, есть способ возбудить процессы аутофагии и без ограничения себя в еде. Для этого необходимо включить в свой рацион некоторые специфические продукты, в которых содержатся активизирующие нужные процессы вещества. Такими продуктами являются (в скобках указаны вещества):
- Сок граната, клубники и малины, а также красное вино, выдержанное в дубовых бочках (уролитин А)
- Грейпфрут, сыр и грибы (спермидин)
- Горькие огурцы (кукурбитацин)
- Соя (диосцин)
- Красный виноград (ресвератрол)
- Карри (куркумин)
- Какао и зеленый чай (катехин и эпикатехин)
- Корень женьшеня (магнофлорин)
- Бурый рис (гамма-токотриенол)
- Грецкие орехи и арахис, шампиньоны, ячмень, бобовые, овес, хлеб и белое мясо (витамин B3)
Также возьмите на заметку овсянку, рыбий жир, айву, оливковое масло, сметану, шпинат, капусту, бруснику, кефир и яйца – вещества, содержащиеся в этих продуктах, стимулируют обновление клеток.
Помимо прочего, примечательно еще и то, что процесс аутофагии запускают не только голодание и правильное питание, а еще и физические нагрузки и спорт. Но чтобы это произошло, нужно придерживаться некоторых принципов.
Аутофагия и спорт
Известно, что эффект от физических упражнений возникает только тогда, когда организм испытывает стресс. Аутофагия возникает по той же самой причине, а потому спорт – это еще один способ ее запуска и усиления.
Физические нагрузки приводят к микроповреждениям тканей и мышц, которые, восстановившись, становятся сильнее, делая более сильным и тело человека. А еще упражнения позволяют очистить организм от токсинов благодаря потению, чего и требует любая детокс-программа. Причем многие специалисты уверены, что именно физические нагрузки служат главным фактором для эффективной детоксикации.
К примеру, доктор Джордж Йу, работающий в медицинском центре Вашингтонского университета и изучающий процессы метаболизма, советует сочетать физические упражнения с посещением сауны, а также принимать добавки ниацина. Так токсины максимально выводятся через кожу, предупреждается возникновение рака и болезни Альцгеймера.
Что касается количества физических упражнений с целью стимулировать аутофагию, то оно пока точно не известно. Но установлено, что наибольшим эффектом обладают интенсивные упражнения, а значит, о легкой нагрузке стоит на время забыть.
Несмотря на то, что долголетию способствуют умеренные нагрузки в объеме 150-450 минут в неделю (они снижают риск преждевременной смерти более чем на 30%), если вы будете уделять хотя бы 30% тренировочного времени на упражнения повышенной интенсивности, то сможете запустить аутофагию и увеличить продолжительность своей жизни еще примерно на 13%. Так что тренируйтесь, не жалея себя (в здоровом смысле, естественно), и мощное улучшение состояния организма не заставит себя долго ждать (при этом не забывайте рассчитывать свои силы и берите во внимание свое текущее физическое состояние).
И, напоследок, еще раз напомним, что аутофагия – это ни в коем случае не лекарство, и считать его панацеей от всех бед нельзя. Вы должны знать о ней и использовать ее, чтобы очистить свой организм и продлить себе жизнь, но делать это нужно с умом, будучи внимательным к своему текущему состоянию и не пренебрегая принципами здорового питания и здорового образа жизни вообще.
При желании вы можете отыскать немало официальных данных, результатов исследований и другой дополнительной информации об аутофагии в интернете. Мы же в свою очередь желаем вам крепкого здоровья и долгих лет жизни!
Что такое аутофагия: механизм, как правильно голодать
Голодать или не голодать – вот в чем вопрос? Если бы шекспировский Гамлет жил в наше время, он бы задумывался не о проблемах бытия, а о том, есть ли смысл устраивать своему организму разгрузочный день. Долгое время никто из специалистов не мог дать четкий и аргументированный ответ на этот вопрос. Некоторые ученые утверждали, что голодовка благотворно влияет на организм человека, другие же пугали среднестатистических граждан, далеких от медицины, рассказами о том, что разгрузочные дни ничего хорошего нашему организму не дадут, а только нанесут ему серьезный вред.
Разобраться в этом вопросе помог японский ученый и специалист по клеточной биологии Ёсинори Осуми, который открыл механизмы аутофагии, детально разобрался в данном процессе и рассказал, как его запустить. За свое открытие в конце 2016 года ученый получил Нобелевскую премию по медицине.
Что же такое аутофагия? Какое отношение она имеет к разгрузочным дням? Почему открытие этого процесса вызвало такой резонанс в мире науки? Как это событие повлияло на методы лечения онкологических заболеваний и заболеваний мозга? Сегодня узнаем ответы на эти важные вопросы.

Аутофагия: что это такое?
Аутофагия (в переводе с древнегреческого «поедание самого себя») – это естественный процесс, который происходит в человеческом организме на клеточном уровне и заключается в удалении дисфункциональных или ненужных компонентов. Все клетки нашего организма обладают возможностью частично «поедать» самих себя, чтобы избавиться от поврежденных или старых участков. Клетка, перерабатывая какую-то часть самой себя, получает новые ресурсы, которые она использует в дальнейшем для восстановления и нормального функционирования.
Если давать определение данному термину более простыми словами, то аутофагия – это процесс избавления и переработки клеткой своих же ненужных частей (клеточных мембран, белков, органоидов). Аутофагию можно назвать процессом, который обеспечивает строительные блоки и необходимую энергию для регенерации клеток.
Подобный феномен ученые обнаружили еще в 60‑х годах прошлого столетия, но только Ёсинори Осуми удалось разобраться в самой сути этого процесса. Японский ученый начал изучать механизмы аутофагии в 1992 году. Специалист изначально изучал гены, которые отвечают за аутофагию в клетках дрожжей. Спустя некоторое время господин Осуми выяснил, что механизмы аутофагии оказывают существенное влияние на различные заболевания человеческого организма: диабет, рак, инфекционные, нейродегенеративные болезни.
Некоторые ученые относят аутофагию к естественным процессам клеточной смерти. Но далеко не все специалисты согласны с таким определением, ведь было проведено множество серьезных исследований, результаты которых подтверждают, что аутофагия — это защитный механизм, позволяющий клеткам при неблагоприятных для них условиях спастись от неминуемой гибели.
Механизм действия аутофагии: как это работает?
Избавление от ненужных и уже выполнивших свою роль клеточных компонентов – это хоть и естественный, но высокорегулируемый процесс, благодаря которому происходит регенерация клеток. Аутофагия не должна выходить из-под контроля, ведь она может нанести непоправимый вред организму. Но не стоит бояться аутофагии, ведь процесс удаления не менее важен, чем процесс созидания, так как построить что-то новое без разрушения старого просто невозможно.
Активизировать аутофагию можно при помощи голодания. Ограничение питательных веществ понижает уровень инсулина в крови, но повышает уровень гормона глюкагона, который стимулирует запуск процесса аутофагии.
Голодание не только запускает в нашем организме процесс аутофагии, но и повышает уровень гормона роста, благодаря чему наш организм начинает активнее продуцировать новые клеточные компоненты, что способствует обновлению нашего тела.
Ненужные клеточные компоненты в процессе аутофагии расщепляются и превращаются в аминокислоты, которые являются строительными блоками для белков. Уровни аминокислот в организме начинают повышаться. Происходит это на ранних стадиях голодания. Ученые утверждают, что полученные таким образом аминокислоты используются организмом для глюконеогенеза, поэтому они направляются в печень. Если же аминокислоты не направляются организмом в печень, то они расщепляются на глюкозу и используются организмом в процессе цикла трикарбоновых кислот или же становятся частью новых белков.
Организм человека, клетки которого накапливают старые белки и не избавляются от них, рано или поздно сталкивается с онкологическими заболеваниями или болезнью Альцгеймера. Тау-белки или бета-амилоиды – аномальные белки, которые скапливаются в клетках и становятся причиной возникновения болезни Альцгеймера. Они негативно влияют на клетки мозга, разрушают их и делают человека слабоумным.

Как правильно запустить процесс аутофагии?
Чтобы запустить процесс аутофагии, необходимо заставить клетки голодать. Тогда они будут использовать не те «стройматериалы», которые поступают извне, а «разбирать» самих себя на части, чтобы все ненужные и непригодные компоненты удалить, а из годных и сильных компонентов создавать обновленный вариант себя.
Голодание активизирует аутофагию, но голодать нужно правильно. Если постоянно существовать в режиме недоедания, то процесс аутофагии не сможет остановиться на нужном вам этапе, что может стать причиной активизации процесса дегенерации.
Существует два вида правильного голодания: пролонгированное и прерывистое. Первый вариант предусматривает отказ от еды на 2 и более дня и недельный перерыв до следующего голодания. Второй вариант предусматривает отказ от еды на сутки и один-два дня нормального питания до следующего отказа от пищи на 24 часа.
Не забывайте, что отказ распространяется на еду, а не на воду.
Процесс аутофагии можно запустить и без голодания, но эффект от него будет не таким заметным. Чтобы сделать это, необходимо ввести в свой рацион продукты, содержащие способствующие аутофагии вещества:
· сок клубники и малины, гранатовый сок, из которых благодаря кишечной микрофлоре образуется уролитин А;
· кисломолочные продукты – витамин D;
· грейпфрут, грибы, сыр – спермидин;
· ячмень, бобовые, овес, шампиньоны, грецкие орехи, арахис, хлеб – витамин В3;
· горькие огурцы – кукурбитацин;
· бурый рис – гамма-токотриенол;
· физалис – физалин А;
· корень женьшеня – магнофлорин;
· соя – диосцин;
· какао, зеленый чай – эпикатехин, катехин;
· красный виноград – ресвератрол;
· карри – куркумин.
Специалисты рекомендуют употреблять указанные выше продукты, чтобы активизировать процесс аутофагии. Но не стоит злоупотреблять ими, иначе можно навредить своему организму.
Как правильно голодать, чтобы активизировать аутофагию?
Пролонгированный тип голодания
Активизировать аутофагию способны циклы пролонгированного голодания. Один цикл должен длиться два и более дня, а перерыв между циклами должен длиться минимум 7 – 8 дней. Во время перерыва питание вызывающего аутофагию человека обязано быть продуманным и сбалансированным.
Проведя многочисленные исследования, ученые доказали, что у людей, практикующих пролонгированное голодание, повысилась чувствительность злокачественных опухолей к терапии, а регулирование уровней инсулиноподобного фактора роста 1, инсулина, глюкозы заметно улучшилось.
Пролонгированное голодание приводит к снижению количества лейкоцитов в крови и массы печени. Но как только человек начинает нормально питаться, его печень восстанавливается, а в иммунной системе запускаются важные процессы возобновления.
Данный вид голодания подходит далеко не всем людям, поэтому практиковать его необходимо только под строгим контролем врача. Людям после 65 лет следует с особой осторожностью использовать этот подход, так как в этом возрасте недостаток белков может спровоцировать нежелательную потерю мышечной массы.
Прерывистый тип голодания
Опыты, которые проводились на лабораторных мышах, подтвердили, что прерывистое голодание является отличной профилактикой сахарного диабета, сердечно-сосудистых, нейродегенеративных, опухолевых заболеваний. У больных бронхиальной астмой людей, которые практиковали двухмесячное голодание в режиме «один день через один день», количество маркеров воспаления заметно снизилось.
Хотя прерывистое голодание не очень сочетается с общепринятой и любимой многими диетологами концепцией дробного питания (кушать понемногу, но часто), но у людей, которые часто едят, уровень инсулина в крови значительно повышается. Постепенно клетки становятся нечувствительными к инсулину, что способствует возникновению инсулеинрезистентности. Через некоторое время у такого человека может развиться сахарный диабет 2‑го типа.
Почему же рекомендации по дробному питанию потеряли свою актуальность? Было проведено несколько исследований на лабораторных мышах. Одну группу мышей кормили с интервалом в двенадцать часов, другая же группа питалась дробно и часто. Представители и первой, и второй группы получали одинаковое количество калорий в сутки. У мышей, которые пытались с интервалом в двенадцать часов, значительно улучшались циркадные ритмы, у них исчезли проблемы со сном, они меньше нервничали и раздражались, а метаболические заболевания не только не развивались дальше, но и исчезали.
Если у вас напряженный рабочий график и вы далеко не всегда успеваете пообедать, то это повод для радости, а не для печали! И старайтесь как можно реже устраивать себе перекусы в разгар рабочего дня.
Ученые утверждают, что питание с интервалами в 12 – 14 часов не только запускает процесс аутофагии, но и снижает уровень глюкозы и вредного холестерина, способствует потере жировой, но не мышечной массы тела. Если же голодать с вечера до утра 13 и более часов, то риск возникновения рака молочной железы уменьшается в несколько раз!
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.


Добавить комментарий