Раствор Натрия Хлорид: инструкция по применению, что это такое, ингаляции, цена
Закрыть- Болезни
- Инфекционные и паразитарные болезни
- Новообразования
- Болезни крови и кроветворных органов
- Болезни эндокринной системы
- Психические расстройства
- Болезни нервной системы
- Болезни глаза
- Болезни уха
- Болезни системы кровообращения
- Болезни органов дыхания
- Болезни органов пищеварения
- Болезни кожи
- Болезни костно-мышечной системы
- Болезни мочеполовой системы
- Беременность и роды
- Болезни плода и новорожденного
- Врожденные аномалии (пороки развития)
- Травмы и отравления
- Симптомы
- Системы кровообращения и дыхания
- Система пищеварения и брюшная полость
- Кожа и подкожная клетчатка
- Нервная и костно-мышечная системы
- Мочевая система
- Восприятие и поведение
- Речь и голос
- Общие симптомы и признаки
- Отклонения от нормы
- Диеты
- Снижение веса
- Лечебные
- Быстрые
- Для красоты и здоровья
- Разгрузочные дни
- От профессионалов
- Монодиеты
- Звездные
- На кашах
- Овощные
- Детокс-диеты
- Фруктовые
- Модные
- Для мужчин
- Набор веса
- Вегетарианство
- Национальные
- Лекарства
- Антибиотики
- Антисептики
- Биологически активные добавки
- Витамины
- Гинекологические
- Гормональные
- Дерматологические
- Диабетические
- Для глаз
- Для крови
- Для нервной системы
- Для печени
- Для повышения потенции
- Для полости рта
- Для похудения
- Для суставов
- Для ушей
- Желудочно-кишечные
- Кардиологические
- Контрацептивы
- Мочегонные
- Обезболивающие
- От аллергии
- От кашля
- От насморка
- Повышение иммунитета
- Противовирусные
- Противогрибковые
- Противомикробные
- Противоопухолевые
- Противопаразитарные
- Противопростудные
- Сердечно-сосудистые
- Урологические
- Другие лекарства
- Врачи
- Клиники
- Справочник
- Аллергология
- Анализы и диагностика
- Беременность
- Витамины
- Вредные привычки
- Геронтология (Старение)
- Дерматология
- Дети
- Женское здоровье
- Инфекция
- Контрацепция
- Косметология
- Народная медицина
- Обзоры заболеваний
- Обзоры лекарств
- Ортопедия и травматология
- Питание
- Пластическая хирургия
- Процедуры и операции
- Психология
- Роды и послеродовый период
- Сексология
- Стоматология
- Травы и продукты
- Трихология
- Другие статьи
- Словарь терминов
- [А] Абазия .. Ацидоз
- [Б] Базофилы .. Булимия
- [В] Вазектомия .. Выкидыш
- [Г] Галлюциногены .. Грязи лечебные
- [Д] Дарсонвализация .. Дофамин
- [Е] Еюноскопия
- [Ж] Железы .. Жиры
- [З] Заместительная гормональная терапия
- [И] Игольный тест .. Искусственная кома
- [К] Каверна .. Кумарин
- [Л] Лапароскоп .. Лучевая терапия
- [М] Магнитотерапия .. Мутация
- [Н] Наркоз .. Нистагм
- [О] Общий анализ крови .. Отек
- [П] Паллиативная помощь .. Пульс
- [Р] Реабилитация .. Родинка (невус)
- [С] Секретин .. Сыворотка крови
Sodium chloride — это… Что такое Sodium chloride?
Хлори́д на́трия — химическое соединение NaCl, натриевая соль соляной кислоты.
Хлорид натрия известен в быту под названием поваренной соли, основным компонентом которой он является. Хлорид натрия в значительном количестве содержится в морской воде, создавая её солёный вкус. Встречается в природе в виде минерала галита (каменная соль).
Чистый хлорид натрия имеет вид бесцветных кристаллов.
Кристаллическая структура

Кристаллическая решётка хлорида натрия.
Голубой цвет = Na+
Зеленый цвет = Cl−
Хлорид натрия образует кристаллы с кубической симметрией. Более крупные ионы хлора образуют плотную кубическую упаковку, в свободных узлах которой (в вершинах правильного октаэдра) расположены ионы натрия.
Умеренно растворяется в воде, растворимость мало зависит от температуры: коэффициент растворимости NaCl (в г на 100 г воды) равен 35,9 при 21° С и 38,1 при 80° С. Растворимость хлорида натрия существенно снижается в присутствии хлороводорода, гидроксида натрия, солей — хлоридов металлов. Растворяется в жидком аммиаке, вступает в реакции обмена.
| Термодинамические характеристики | |
|---|---|
| ΔfH0g | −181,42 кДж/моль |
| ΔfH0l | −385,92 кДж/моль |
| ΔfH0s | −411,12 кДж/моль |
| ΔfH0aq | −407 кДж/моль |
| S0g, 1 bar | 229,79 Дж/(моль K) |
| S0l, 1 bar | 95,06 Дж/(моль K) |
| S0s | 72,11 Дж/(моль•K) |
Диэлектрическая проницаемость NaCl — 6,3
См. также
Wikimedia Foundation. 2010.
Гипохлорит натрия — Википедия
| Гипохлорит натрия | |
|---|---|
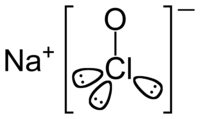 ( {{{картинка}}}) | |
| Систематическое наименование | Гипохлорит натрия |
| Традиционные названия | Гипохлорит натрия, лабарракова вода, жавелевая вода[К 1] |
| Хим. формула | NaOCl |
| Рац. формула | NaOCl |
| Молярная масса | 74,443 г/моль |
| Плотность | пентагидрат: 1,574[1] г/см³; 1,1[2] |
| Температура | |
| • плавления | NaOCl · 5H2O[К 2]: 24,4 °C; NaOCl · 2,5H2O: 57,5[3] |
| • разложения | 5%-й раствор[2]: 40 °C |
| Энтальпия | |
| • образования | пентагидрат[К 3]: − 350,4[3] кДж/моль |
| Растворимость | |
| • в воде | NaOCl · 5H2O (20 °C): 53,4[4] |
| • в воде | NaOCl · 2,5H2O (50 °C): 129,9[4] |
| Рег. номер CAS | 7681-52-9 |
| PubChem | 23665760 |
| Рег. номер EINECS | 231-668-3 |
| SMILES | |
| InChI | |
| RTECS | Nh4486300 |
| ChEBI | 32146 |
| Номер ООН | 1791 |
| ChemSpider | 22756 |
| Токсичность | Едкий, окислитель, токсичный, опасность для окружающей среды |
| Пиктограммы СГС |     |
| NFPA 704 |  |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |
Гипохлори́т на́трия (натрий хлорноватистокислый) — NaOCl[К 4], неорганическое соединение, натриевая соль хлорноватистой кислоты. Тривиальное (историческое) название водного раствора соли — «лабарракова вода» или «жавелевая вода»[К 1].
Соединение в свободном состоянии очень неустойчиво, обычно используется в виде относительно стабильного пентагидрата NaOCl · 5H2O или водного раствора, имеющего характерный резкий запах хлора и обладающего высокими коррозионными свойствами.
Соединение — сильный окислитель, содержит 95,2 % активного хлора[К 5]. Обладает антисептическим и дезинфицирующим действием. Используется в качестве бытового и промышленного отбеливателя и дезинфектанта, средства очистки и обеззараживания воды, окислителя для некоторых процессов промышленного химического производства. Как бактерицидное и стерилизующее средство применяется в медицине, пищевой промышленности и сельском хозяйстве.
По мнению издания The 100 Most Important Chemical Compounds (Greenwood Press, 2007)[2], гипохлорит натрия входит в сотню самых важных химических соединений.
В 1774 году шведским химиком Карлом Вильгельмом Шееле был открыт хлор[5]. Спустя 11 лет в 1785 году (по другим данным — в 1787 году[2]), другой химик, француз Клод Луи Бертолле, обнаружил, что водный раствор этого газа (см. уравнение (1)) обладает отбеливающими свойствами[6][К 6].
- Cl2+h3O=HCl+HOCl (1){\displaystyle {\mathsf {Cl_{2}+H_{2}O=HCl+HOCl}}\ \ \ \ (1)}
Небольшое Парижское предприятие Societé Javel, открытое в 1778 году на берегах Сены и возглавляемое Леонардом Альбаном (англ. Leonard Alban), адаптировало открытие Бертолле к промышленным условиям и начало выпуск белильной жидкости, растворяя газообразный хлор в воде. Однако получаемый продукт был очень нестабильным, поэтому в 1787 году процесс был модифицирован. Хлор стали пропускать через водный раствор поташа (карбоната калия) (см. уравнение
- Cl2+2K2CO3+h3O=2KHCO3+KOCl+KCl (2){\displaystyle {\mathsf {Cl_{2}+2K_{2}CO_{3}+H_{2}O=2KHCO_{3}+KOCl+KCl}}\ \ \ \ (2)}
В 1820 году французский аптекарь Антуан Лабаррак (фр. Antoine Germain Labarraque) заменил поташ на более дешёвую каустическую соду (гидроксид натрия) (см. уравнение (3)). Получившийся раствор гипохлорита натрия получил название «Eau de Labarraque» («лабарракова вода»). Он стал широко использоваться для отбеливания и дезинфекции[7].
- Cl2+2NaOH=NaCl+NaOCl+h3O (3){\displaystyle {\mathsf {Cl_{2}+2NaOH=NaCl+NaOCl+H_{2}O}}\ \ \ \ (3)}
Несмотря на то, что дезинфицирующие свойства гипохлорита были обнаружены в первой половине XIX века, использование его для обеззараживания питьевой воды и очистки сточных вод началось только в конце века. Первые системы водоочистки были открыты в 1893 году в Гамбурге[2]; в США первый завод по производству очищенной питьевой воды появился в 1908 году в Джерси-Сити[8].
Безводный гипохлорит натрия представляет собой неустойчивое бесцветное кристаллическое вещество. Элементный состав: Na (30,9 %), Cl (47,6 %), O (21,5 %).
Хорошо растворим в воде: 53,4 г в 100 граммах воды (130 г на 100 г воды при 50 °C)[9].
У соединения известно три кристаллогидрата:
- моногидрат NaOCl · H2O — крайне неустойчив, разлагается выше 60 °C, при более высоких температурах — со взрывом[3].
- NaOCl · 2,5H2O — более устойчив, плавится при 57,5 °C[3].
- пентагидрат NaOCl · 5H2O — наиболее устойчивая форма, представляет собой бледно-зеленовато-жёлтые (технического качества — белые[10]) ромбические кристаллы (a = 0,808 нм, b = 1,606 нм, c = 0,533 нм, Z = 4). Не гигроскопичен, хорошо растворим в воде (в г/100 граммов воды, в пересчёте на безводную соль): 26 (−10 °C), 29,5 (0 °C), 38 (10 °C), 82 (25 °C), 100 (30 °C). В воздухе расплывается, переходя в жидкое состояние, из-за быстрого разложения[3]. Температура плавления: 24,4 °C (по другим данным: 18 °C[10]), при нагревании (30—50 °C) разлагается[1].
Плотность водного раствора гипохлорита натрия при 18 °C[11]:
| 1 % | 2 % | 4 % | 6 % | 8 % | 10 % | 14 % | |
|---|---|---|---|---|---|---|---|
| Плотность, г/л | 1005,3 | 1012,1 | 1025,8 | 1039,7 | 1053,8 | 1068,1 | 1097,7 |
| 18 % | 22 % | 26 % | 30 % | 34 % | 38 % | 40 % | |
| 1128,8 | 1161,4 | 1195,3 | 1230,7 | 1268,0 | 1308,5 | 1328,5 |
Температура замерзания водных растворов гипохлорита натрия различных концентраций[12]:[стр. 458]:
| 0,8 % | 2 % | 4 % | 6 % | 8 % | 10 % | 12 % | 15,6 % | |
|---|---|---|---|---|---|---|---|---|
| Температура замерзания, °C | −1,0 | −2,2 | −4,4 | −7,5 | −10,0 | −13,9 | −19,4 | −29,7 |
Термодинамические характеристики гипохлорита натрия в бесконечно разбавленном водном растворе[13]:
Разложение и диспропорционирование[править | править код]
Гипохлорит натрия — неустойчивое соединение, легко разлагающееся с выделением кислорода:
- 2NaOCl=2NaCl+O2{\displaystyle {\mathsf {2NaOCl=2NaCl+O_{2}}}}
Самопроизвольное разложение медленно происходит даже при комнатной температуре: за 40 суток пентагидрат (NaOCl · 5H2O) теряет 30 % активного хлора[К 5][13]. При температуре 70 °C разложение безводного гипохлорита протекает со взрывом[14].
При нагревании параллельно происходит реакция диспропорционирования[13]:
- 3NaOCl=NaClO3+2NaCl{\displaystyle {\mathsf {3NaOCl=NaClO_{3}+2NaCl}}}
Гидролиз и разложение в водных растворах[править | править код]
Растворяясь в воде, гипохлорит натрия диссоциирует на ионы:
- NaOCl →h3O Na++OCl−{\displaystyle {\mathsf {NaOCl\ {\xrightarrow {H_{2}O}}\ Na^{+}+OCl^{-}}}}
Так как хлорноватистая кислота (HOCl) очень слабая (pKa = 7,537[13]), гипохлорит-ион в водной среде подвергается гидролизу:
- OCl−+h3O⇆HOCl+OH−{\displaystyle {\mathsf {OCl^{-}\!+H_{2}O\leftrightarrows HOCl+OH^{-}}}}
Именно наличие хлорноватистой кислоты в водных растворах гипохлорита натрия объясняет его сильные дезинфицирующие и отбеливающие свойства[13] (см. раздел «Физиологическое действие и воздействие на окружающую среду»).
Водные растворы гипохлорита натрия неустойчивы и со временем разлагаются даже при обычной температуре (0,085 % в сутки[3]). Распад ускоряет освещение, ионы тяжёлых металлов и хлориды щелочных металлов; напротив, сульфат магния, ортоборная кислота, силикат и гидроксид натрия замедляют процесс; при этом наиболее устойчивы растворы с сильнощелочной средой (pH > 11)[3].
В сильнощелочной среде (pH > 10), когда гидролиз гипохлорит-иона подавлен, разложение происходит следующим образом[15]:
- 2OCl−=2Cl−+O2{\displaystyle {\mathsf {2OCl^{-}\!=2Cl^{-}\!+O_{2}}}}
При температурах выше 35 °C распад сопровождается реакцией диспропорционирования[15]:
- 3OCl−=2Cl−+ClO3−{\displaystyle {\mathsf {3OCl^{-}\!=2Cl^{-}\!+ClO_{3}^{-}}}}
При диапазоне pH от 5 до 10, когда концентрация хлорноватистой кислоты в растворе становится заметной, разложение идёт по следующей схеме[15]:
- HOCl+2ClO−=ClO3−+2Cl−+H+{\displaystyle {\mathsf {HOCl+2ClO^{-}=ClO_{3}^{-}+2Cl^{-}+H^{+}}}}
- HOCl+ClO−=O2+2Cl−+H+{\displaystyle {\mathsf {HOCl+ClO^{-}\!=O_{2}+2Cl^{-}\!+H^{+}}}}
В кислой среде разложение HOCl ускоряется, а в очень кислой среде (pH < 3) при комнатной температуре наблюдается распад по следующей схеме[13]:
- 4HOCl=2Cl2+O2+2h3O{\displaystyle {\mathsf {4HOCl=2Cl_{2}+O_{2}+2H_{2}O}}}
Если для подкисления используется соляная кислота, в результате выделяется хлор:
- NaOCl+2HCl=NaCl+Cl2↑+h3O{\displaystyle {\mathsf {NaOCl+2HCl=NaCl+Cl_{2}\!\uparrow \!+H_{2}O}}}
Пропуская через охлаждённый водный раствор гипохлорита натрия углекислый газ, можно получить раствор хлорноватистой кислоты:
- NaOCl+h3O+CO2=NaHCO3↓+HOCl{\displaystyle {\mathsf {NaOCl+H_{2}O+CO_{2}=NaHCO_{3}\!\downarrow \!+HOCl}}}
Окислительные свойства[править | править код]
Водный раствор гипохлорита натрия — сильный окислитель, вступающий в многочисленные реакции с разнообразными восстановителями, независимо от кислотно-щелочного характера среды[16].
Рассмотрим основные варианты развития окислительно-восстановительного процесса и стандартные электродные потенциалы полуреакций в водной среде[17][К 7]:
- в кислой среде:
- NaOCl+H+=Na++HOCl{\displaystyle {\mathsf {NaOCl+H^{+}=Na^{+}+HOCl}}}
| 2HOCl+2H++2e−=Cl2↑+2h3O{\displaystyle {\mathsf {2HOCl+2H^{+}\!+2e^{-}=Cl_{2}\!\uparrow \!+2H_{2}O}}} | Eo=1,630B{\displaystyle E^{o}{\mathsf {=1,630B}}} |
| HOCl+H++2e−=Cl−+h3O{\displaystyle {\mathsf {HOCl+H^{+}\!+2e^{-}=Cl^{-}\!+H_{2}O}}} | Eo=1,500B{\displaystyle E^{o}{\mathsf {=1,500B}}} |
- в нейтральной и щелочной среде:
| OCl−+h3O+2e−=Cl−+2OH−{\displaystyle {\mathsf {OCl^{-}\!+H_{2}O+2e^{-}=Cl^{-}\!+2OH^{-}}}} | Eo=0,890B{\displaystyle E^{o}{\mathsf {=0,890B}}} |
| 2OCl−+2h3O+2e−=Cl2↑+ 4OH−{\displaystyle {\mathsf {2OCl^{-}\!+2H_{2}O+2e^{-}=Cl_{2}\!\uparrow \!+\ 4OH^{-}}}} | Eo=0,421B{\displaystyle E^{o}{\mathsf {=0,421B}}} |
Некоторые окислительно-восстановительные реакции с участием гипохлорита натрия:
- NaOCl+2NaI+h3O=NaCl+I2+2NaOH{\displaystyle {\mathsf {NaOCl+2NaI+H_{2}O=NaCl+I_{2}+2NaOH}}}
- 3NaOCl+NaI=3NaCl+NaIO3{\displaystyle {\mathsf {3NaOCl+NaI=3NaCl+NaIO_{3}}}}
- 4NaOCl+NaI=4NaCl+NaIO4{\displaystyle {\mathsf {4NaOCl+NaI=4NaCl+NaIO_{4}}}}
- NaOCl+K2SO3=NaCl+K2SO4{\displaystyle {\mathsf {NaOCl+K_{2}SO_{3}=NaCl+K_{2}SO_{4}}}}
- 2NaOCl+Ca(NO2)2=2NaCl+Ca(NO3)2{\displaystyle {\mathsf {2NaOCl+Ca(NO_{2})_{2}=2NaCl+Ca(NO_{3})_{2}}}}
- NaOCl+NaOH+HCOONa=NaCl+Na2CO3+h3O{\displaystyle {\mathsf {NaOCl+NaOH+HCOONa=NaCl+Na_{2}CO_{3}+H_{2}O}}}
- 2As+6NaOH+5NaOCl=2Na3AsO4+5NaCl+3h3O{\displaystyle {\mathsf {2As+6NaOH+5NaOCl=2Na_{3}AsO_{4}+5NaCl+3H_{2}O}}}
- Аммиак под действием гипохлорита натрия через с
Sodium chloride / натрия хлорид инструкция по применению, противопоказания, побочные эффекты, отзывы medistok.ru — жизнь без болезней и лекарств medistok.ru

Препарат для регидратации и дезинтоксикации.
Активное вещество препарата: SODIUM CHLORIDE / НАТРИЯ ХЛОРИД
Фармакологическое действие Sodium chloride / натрия хлорид
Ионы натрия и хлора являются важнейшими неорганическими компонентами внеклеточной жидкости, поддерживающими соответствующее осмотическое давление плазмы крови и внеклеточной жидкости. Изотонический раствор восполняет дефицит жидкости в организме при дегидратации. Гипертонический раствор натрия хлорида при в/в введении обеспечивает коррекцию осмотического давления внеклеточной жидкости и плазмы крови. При местном применении в офтальмологии натрия хлорид оказывает противоотечное действие.
Фармакокинетика препарата.
—
Показания к применению:
Изотонический раствор: дегидратация различного генеза. Для поддержания объема плазмы крови во время и после операций. В качестве растворителя для различных препаратов.
Гипертонический раствор: нарушения водно-электролитного обмена: дефицит ионов натрия и хлора; гипоосмолярная дегидратация различного генеза (вследствие длительной рвоты, диареи, ожогов; при желудочной фистуле, легочном кровотечении, кишечном кровотечении).
Глазные капли и мазь: раздражение роговицы при воспалительных и аллергических заболеваниях (в составе комбинированной терапии).
Дозировка и способ применения препарата.
Изотонический раствор натрия хлорида вводят в/в, п/к и в клизмах, а также используют для промывания ран, глаз, слизистой носовой полости. Чаще вводят в/в, в зависимости от клинической ситуации — до 3 л/сут.
Гипертонический раствор натрия хлорида вводят в/в. Разовая доза для в/в струйного введения может составлять 10-30 мл. При состояниях, требующих немедленного восполнения ионов натрия и хлора, препарат вводят в/в капельно в дозе 100 мл.
Местно и наружно применяют в зависимости от используемой лекарственной формы и схемы лечения.
Побочное действие Sodium chloride / натрия хлорид:
Возможно: тошнота, рвота, диарея, спазмы желудка, жажда, слезотечение, потливость, лихорадка, тахикардия, артериальная гипертензия, нарушение функции почек, отеки, одышка, головная боль, головокружение, беспокойство, слабость, подергивание и гипертонус мышц.
При наружном и местном применении побочные реакции к настоящему времени не установлены.
Противопоказания к препарату:
Гипернатриемия, состояния гипергидратации, угроза отека легких, мозга.
Особый указания по применению Sodium chloride / натрия хлорид.
С осторожностью применяют большие объемы натрия хлорида у пациентов с нарушением выделительной функции почек, при гипокалиемии. Введение больших количеств раствора может привести к хлоридному ацидозу, гипергидратации, увеличению выведения калия из организма.
Гипертонический раствор не применяют п/к и в/м.
При длительном применении необходим контроль концентрации электролитов в плазме и суточного диуреза.
Температура инфузионного раствора должна составлять 38°С.
Взаимодействие Sodium chloride / натрия хлорид с другими препаратами.
—
Натрия Хлорид (Sodium Chloride) — это… Что такое Натрия Хлорид (Sodium Chloride)?
- Натрия Хлорид (Sodium Chloride)
- обычная поваренная соль: натриевая соль, которая присутствует во всех тканях и необходима для поддержания в организме нормального электролитного баланса. Внутривенное введение хлорида натрия является основой инфузионной заместительной терапии, проводимой после выполнения различных операций или в случае сильного истощения запасов натрия в организме, возникающего, например, во время шока или обезвоживания. Хлорид натрия является основным компонентом при проведении оральной регидратационной терапии.
Источник: «Медицинский словарь»
Медицинские термины. 2000.
- Натрия Фусидат (Sodium Fusidate)
- Натуропатия (Naturopathy)
Смотреть что такое «Натрия Хлорид (Sodium Chloride)» в других словарях:
Натрия хлорид — Действующее вещество ›› Натрия хлорид (Sodium chloride) Латинское название Sodium chloride АТХ: ›› B05CB01 Натрия хлорид Фармакологические группы: Регуляторы водно электролитного баланса и КЩС ›› Вспомогательные вещества, реактивы и полупродукты… … Словарь медицинских препаратов
Натрия хлорид Биеффе — Действующее вещество ›› Натрия хлорид (Sodium chloride) Латинское название Sodium chloride Bieffe АТХ: ›› B05CB01 Натрия хлорид Фармакологическая группа: Регуляторы водно электролитного баланса и КЩС Состав и форма выпуска 1000 мл раствора для… … Словарь медицинских препаратов
Sodium chloride — Хлорид натрия Общие Систематическое наименование хлорид натрия / Sodium chloride Химическая формула NaCl Молярная масса 58.44277 г/м … Википедия
Натрия хлорид — Хлорид натрия Общие Систематическое наименование хлорид натрия / Sodium chloride Химическая формула NaCl Молярная масса 58.44277 г/м … Википедия
НАТРИЯ ХЛОРИД — (sodium chloride) обычная поваренная соль: натриевая соль, которая присутствует во всех тканях и необходима для поддержания в организме нормального электролитного баланса. Внутривенное введение хлорида натрия является основой инфузионной… … Толковый словарь по медицине
натрия хлорид — natrio chloridas statusas T sritis chemija formulė NaCl atitikmenys: angl. common salt; sodium chloride; table salt rus. натрий хлористый; натрия хлорид; пищевая соль; поваренная соль ryšiai: sinonimas – valgomoji druska … Chemijos terminų aiškinamasis žodynas
sodium chloride — natrio chloridas statusas T sritis chemija formulė NaCl atitikmenys: angl. common salt; sodium chloride; table salt rus. натрий хлористый; натрия хлорид; пищевая соль; поваренная соль ryšiai: sinonimas – valgomoji druska … Chemijos terminų aiškinamasis žodynas
Натрия хлорида изотонический раствор для инъекций 0,9% — Действующее вещество ›› Натрия хлорид (Sodium chloride) … Словарь медицинских препаратов
Хлорид натрия — Хлорид натрия … Википедия
Составной натрия лактат — Действующее вещество ›› Натрия лактата раствор сложный [Калия хлорид + Кальция хлорид + Натрия хлорид + Натрия лактат] (Compound solution of sodium lactate [Potassium chloride + Calcium chloride + Sodium chloride + Sodium lactate]) Латинское… … Словарь медицинских препаратов
sodium chloride — с английского на русский
sodium chloride — n an ionic crystalline chemical compound consisting of equal numbers of sodium and chlorine atoms: SALT (1a) * * * common salt: a salt of sodium that is present in all tissues and is important in maintaining the electrolyte balance of the body.… … Medical dictionary
Sodium chloride — Sodium So di*um, n. [NL., fr.E. soda.] (Chem.) A common metallic element of the alkali group, in nature always occuring combined, as in common salt, in albite, etc. It is isolated as a soft, waxy, white, unstable metal, so highly reactive that it … The Collaborative International Dictionary of English
sodium chloride — n [U] technical the type of salt that is used in cooking … Dictionary of contemporary English
sodium chloride — noun uncount TECHNICAL salt … Usage of the words and phrases in modern English
sodium chloride — ► NOUN ▪ the chemical name for common salt … English terms dictionary
sodium chloride — n. common salt, NaCl … English World dictionary
Sodium chloride — NaCl redirects here. For the Google technology, see Google Native Client. This article is about the chemical compound. For sodium chloride in the diet, see Salt. For sodium chloride as a mineral, see Halite. Sodium chloride … Wikipedia
sodium chloride — noun a white crystalline solid consisting mainly of sodium chloride (NaCl) • Syn: ↑common salt • Hypernyms: ↑binary compound • Hyponyms: ↑halite, ↑rock salt … Useful english dictionary
sodium chloride — common salt: a salt of sodium that is present in all tissues and is important in maintaining the electrolyte balance of the body. Sodium chloride infusions are the basis of fluid replacement therapy after operations and for conditions associated… … The new mediacal dictionary
Sodium chloride — Хлорид натрия Общие Систематическое наименование хлорид натрия / Sodium chloride Химическая формула NaCl Молярная масса 58.44277 г/м … Википедия
sodium chloride — noun Sodium chloride is used before these nouns: ↑solution … Collocations dictionary
SODIUM CHLORIDE — перевод на русский c примерами предложений
ADRIC: Uh. Could anyone pass the sodium chloride, please?
Э. Мог бы кто-нибудь передать хлорид натрия, пожалуйста?
Dalton would have known that table salt, sodium chloride, is always made up of one part sodium and one part chlorine.
Дальтон выяснил, что обычная поваренная соль, хлорид натрия, всегда состоит из одной части натрия и одной части хлора.
In this case, the inert gas is introduced by water from a bromine vial, so a sodium chloride tube isn’t needed.
В этом случае, инертный газ введен водным путем от пузырька брома, таким образом, хлорид натрия не понадобится.
Показать ещё примеры для «хлорид натрия»…
Does this contain enough sodium chloride for your taste?
Хлорида натрия достаточно на твой вкус?
Actually, uh, what you’re looking at is a concentrated mixture of mucus, Tyrosinase, Lysine and Sodium Chloride.
Вообще-то, то на что вы смотрите, это концентрированная смесь слизи, тирозиназа, лизина, и хлорида натрия.
Now, this type of rock salt, it’s composed of sodium chloride and contains traces of cyanide.
Этот тип соли состоит из хлорида натрия и содержит следы цианида.
So, uh, what I found was a combination of hydrochloric acid, potassium chloride and sodium chloride, or more commonly known as gastric acid.
Я нашёл соединение соляной кислоты, хлорида калия и хлорида натрия, всё это, более известно, как желудочный сок.
Sodium chloride.
— Как? Хлоридом натрия.
They’re made up of sodium ferrocyanide mixed with sodium chloride, which means…
Это ферроцианид натрия, смешанный с хлоридом натрия, что означает…

Добавить комментарий